1. Nguyên tố hoá học là gì?
Nguyên tố hoá học là tập hợp các nguyên tử có cùng số điện tích hạt nhân.
Hiện nay người ta đã biết 118 nguyên tố hoá học (94 nguyên tố tồn tại trong tự nhiên + 24 nguyên tố tạo ra trong phòng thí nghiệm).
2. Đồng vị là gì?
Các đồng vị của một nguyên tố hoá học là các nguyên tử có cùng số proton (cùng số Z), khác nhau số neutron (khác số N) => khác số khối A.
Ví dụ: Hydrogen có 3 đồng vị : \({}_{\rm{1}}^{\rm{1}}{\rm{H}}\) (kí hiệu là H), \({}_{\rm{1}}^2{\rm{H}}\) (kí hiệu là D), \({}_{\rm{1}}^3{\rm{H}}\) (kí hiệu là T) ; carbon có 3 đồng vị : \({}_{\rm{6}}^{{\rm{12}}}{\rm{C}}\),\({}_{\rm{6}}^{{\rm{13}}}{\rm{C}}\),\({}_{\rm{6}}^{{\rm{14}}}{\rm{C}}\)
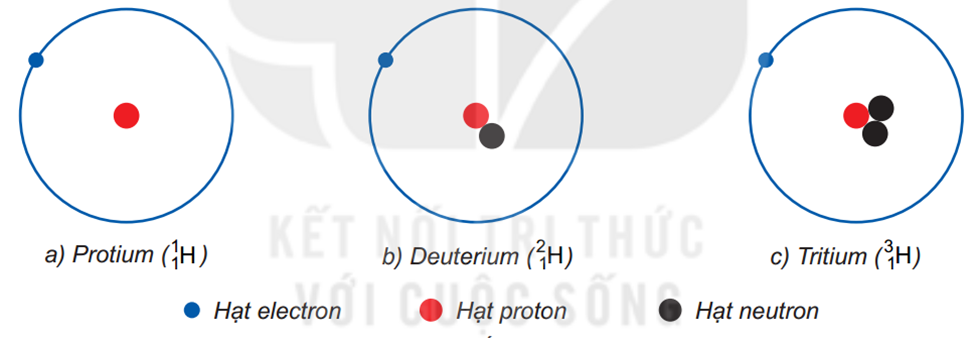
Mô hình cấu tạo nguyên tử các đồng vị của nguyên tố hydrogen
Các đồng vị khác nhau về tính chất vật lí nhưng giống nhau về tính chất hoá học.
Các đồng vị không bền là đồng vị phóng xạ được dung trong y học, nông nghiệp, nghiên cứu khoa học.

 Cấu tạo nguyên tử - Từ điển Hoá 10
Cấu tạo nguyên tử - Từ điển Hoá 10 






Danh sách bình luận