1. Dẫn xuất halogen là gì?
Khi thay thế nguyên tử hydrogen trong phân tử hydrocarbon bằng nguyên tử halogen ta thu được dẫn xuất halogen của hydrocarbon (gọi tắt là dẫn xuất halogen).
2. Tính chất vật lí
- Ở nhiệt độ thường, một số dẫn xuất halogen có phân tử khối nhỏ như CH3F, CH3Cl, CH3Br, C2H5Cl, C3H7F ở trạng thái khí; các dẫn xuất lớn hơn ở trạng thái lỏng hoặc rắn.
- Các dẫn xuất halogen hầu như không tan trong nước, tan tốt trong các dung môi hữu cơ.
- Nhiệt độ nóng chảy và nhiệt độ sôi cao hơn so với hydrocarbon có phân tử khối tương đương do dẫn xuất halogen phân cực.
- Với các dẫn xuất của các halogen khác nhau cùng số C thì nhiệt độ sôi tăng dần từ dẫn xuất của F → Cl → Br → I do phân tử khối tăng dần, tương tác van der walls tăng dần.
3. Phản ứng thế nguyên tử halogen bằng nhóm OH
- Các dẫn xuất halogen mà nguyên tử halogen gắn vào nguyên tử C no có phản ứng thế nhóm -OH trong dung dịch kiềm khi đun nóng tạo alcohol.
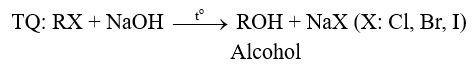
4. Phản ứng tách hydrogen halide (HX)
Trong phản ứng tách hydrogen halide (HX) ra khỏi dẫn xuất halogen, nguyên tử halogen (X) ưu tiên tách ra cùng nguyên tử hydrogen (H) ở carbon carbon bên cạnh bậc cao hơn tạo sản phẩm chính. - Các dẫn xuất monohalogen của alkane bị tách HX khi đun nóng với KOH/C2H5OH tạo alkene.
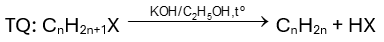
- Qui tắc zaitsev (Zai - xép): Trong phản ứng tách hydrogen halide (HX) ra khỏi dẫn xuất halogen, nguyên tử halogen (X) ưu tiên tách ra cùng nguyên tử hydrogen (H) ở carbon carbon bên cạnh bậc cao hơn tạo sản phẩm chính.

 Dẫn xuất halogen - Alcohol - Phenol - Từ điển Hoá 11
Dẫn xuất halogen - Alcohol - Phenol - Từ điển Hoá 11 






Danh sách bình luận