1. Alcohol là gì?
- Alcohol là những hợp chất hữu cơ trong phân tử chứa nhóm hydroxyl (-OH) liên kết trực tiếp với nguyên tử carbon no.
Điều kiện tồn tại của alcohol: Nhóm -OH phải gắn vào nguyên tử Cno, mỗi C gắn tối đa 1 -OH.
2. Đặc điểm cấu tạo
- Trong phân tử alcohol, liên kết O – H và C – O đều phân cực về phía O nên trong các phản ứng hoá học alcohol thường bị phân cắt ở liên kết O – H và C – O.
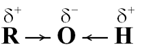
3. Tính chất vật lí
- Ở điều kiện thường, các alcohol no, đơn chức từ C1 đến C12 ở trạng thái lỏng, từ C13 trở lên ở trạng thái rắn. Các polyalcohol như C2H4(OH)2, C3H5(OH)3 là chất lỏng sánh, nặng hơn nước và có vị ngọt.
- Giữa các alcohol có liên kết hydrogen liên phân tử làm tăng nhiệt độ sôi nên alcohol có nhiệt độ sôi cao hơn so với hydrocarbon, dẫn xuất halogen có phân tử khối tương đương.
- Các alcohol từ C1 đến C3 tan vô hạn trong nước do tạo liên kết hydrogen với nước, khi số C tăng thì độ tan giảm do phần gốc hydrocarbon là phần kị nước tăng.
- Độ cồn (độ alcohol) là số mL ethanol nguyên chất có trong 100 mL dung dịch ethanol và H2O:
\(\frac{{{V_{{C_2}{H_5}OHn/c}}}}{{{V_{dd}}}}.100\)
4. Phản ứng thế H của nhóm OH
- Alcohol có phản ứng với Na, K giải phóng khí H2.
TQ: R(OH)a+ aNa → R(ONa)a+ \(\frac{a}{2}\)H2↑
5. Phản ứng tạo ether
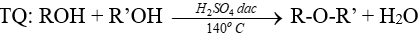
Chú ý: Cho n alcohol đơn chức tách nước sẽ tạo tối đa \(\frac{{n(n + 1)}}{2}\) ether.
6. Phản ứng tách nước tạo alkene
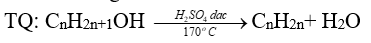
- Phản ứng tách nước của alcohol cũng tuân theo qui tắc tách Zaitsev: OH tách ưu tiên với H của C bên cạnh có bậc cao hơn.
7. Phản ứng oxi hoá
(a) Phản ứng oxi hoá không hoàn toàn
- Các alcohol bị oxi hoá không hoàn toàn bởi CuO khi đun nóng.
+ Alcohol bậc I bị oxi hoá thành aldehyde: 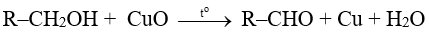
+ Alcohol bậc II bị oxi hoá thành ketone:
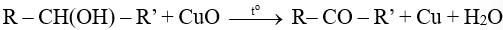
+ Alcohol bậc III không bị oxi hoá bởi CuO, to.
(b) Phản ứng oxi hoá hoàn toàn (PƯ cháy)
- Đối với alcohol no, đơn chức, mạch hở: 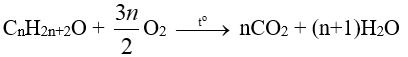
8. Phản ứng riêng của polyalcohol
- Các alcohol đa chức có ít nhất 2 nhóm OH cạnh nhau có khả năng hoà tan Cu(OH)2 ở nhiệt độ thường tạo phức chất màu xanh lam thẫm.
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
glycerol (kết tủa xanh lam) (phức tan, xanh lam thẫm)
- Phản ứng này dùng để nhận biết alcohol đa chức có ít nhất 2OH cạnh nhau.

 Dẫn xuất halogen - Alcohol - Phenol - Từ điển Hoá 11
Dẫn xuất halogen - Alcohol - Phenol - Từ điển Hoá 11 






Danh sách bình luận