Lý thuyết Sulfuric acid và muối sulfate - Hóa học 11 - Kết nối tri thức
- Sulfuric acid là chất lỏng sánh như dầu, không màu, không bay hơi, có tính hút ẩm mạnh. - Tan vô hạn trong nước và tỏa rất nhiều nhiệt. - Cách pha loãng sulfuric acid đặc: rót từ từ dung dịch sulfuric acid đặc vào nước, vừa rót vừa khuấy đều. + Chú ý: Không làm ngược lại.
I. Sulfuric acid
1. Cấu tạo phân tử
- Phân tử H2SO4 có công thức cấu tạo:
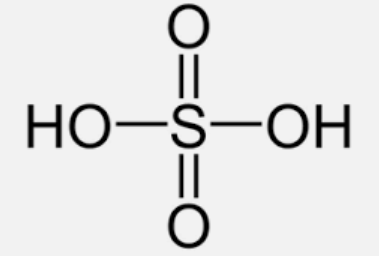
- Liên kết hydrogen giữa các phân tử sulfuric acid:

2. Tính chất vật lí
- Sulfuric acid là chất lỏng sánh như dầu, không màu, không bay hơi, có tính hút ẩm mạnh.
- Tan vô hạn trong nước và tỏa rất nhiều nhiệt.
- Cách pha loãng sulfuric acid đặc: rót từ từ dung dịch sulfuric acid đặc vào nước, vừa rót vừa khuấy đều.
+ Chú ý: Không làm ngược lại.
3. Quy tắc an toàn
a, Bảo quản
- Bảo quản trong chai, lọ có nút đậy chặt.
- Đặt các xa các lọ chứa chất dễ cháy nổ như permanganate, dichromate…
b, Sử dụng
Khi sử dụng tuân thủ các nguyên tắc:
- Sử dụng găng tay, đeo kính bảo hộ, mặc áo thí nghiệm.
- Cầm dụng cụ chắc chắn, thao tác cẩn thận.
- Không tì, đè chai đựng acid lên miệng cốc, ống đông khi rót acid.
- Sử dụng lượng acid vừa phải, lượng acid còn thửa phải thu hồi vào lọ đựng.
- Không được đổ nước vào dung dịch acid đặc.
c, Sơ cứu khi bỏng acid
- Nhanh chóng rửa ngay với nước lạnh nhiều lần.
- Trung hòa acid bằng dung dịch NaHCO3 loãng (2%).
- Băng bó tạm thời bằng băng sạch, uống bù nước điện giải rồi đưa đến cơ sở y tết gần nhất.
4. Tính chất hóa học
a, Dung dịch sulfuric acid loãng
- Có đầy đủ tính chất của một acid mạnh.
+ Làm quỳ tím chuyển sang màu đỏ.
+ Tác dụng với kim loại.
+ Tác dụng với oxide base.
+ Tác dụng với base.
+ Tác dụng với muối.
b, Dung dịch sulfuric acid đặc
- Tính acid: Có tính acid mạnh, được sử dụng để chiều chế một số acid dễ bay hơi.
VD: CaF2 + H2SO4 → CaSO4 + 2HF
- Tính oxi hóa: Có tính oxi hóa mạnh.
+ Sulfuric acid đặc, nóng oxi hóa được nhiều kim loại, phi kim và hợp chất.
VD:
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
C + H2SO4 → CO2 + 2SO2 + 2H2O
2KBr + 2H2SO4 → K2SO4 + Br2 + SO2 + 2H2O
- Tính háo nước: H2SO4 đặc có khả năng lấy nước từ hợp chất carbohydrate và khiến chúng hóa đen.
5. Ứng dụng
- Sản xuất phân bón.
- Sản xuất chất tẩy rửa.
- Chế biến dầu mỏ.
- Sản xuất muối, acid.
…
6. Sản xuất
- GĐ 1: Sản xuất sulfur dioxide.
S(s) +O2(g) → SO2(g)
4FeS2(s) + 11O2(g) → 2Fe2O3(s) + 8SO2(g)
- GĐ 2: Sản xuất sulfur trioxide.
2SO2(g) + O2(g) → 2SO3(g)
- GĐ 3: Hấp thu sulfur trioxide bằng sulfuric acid đặc, tạo ra oleum.
II. Muối sulfate
1. Ứng dụng
- Sản xuất phân đạm.
- Sản xuất thạch cao.
- Sản xuất chất cản quang.
- Sản xuất thạch cao.
- Sản xuất khoảng chất bổ sung cho phân bón, thức ăn gia súc.
2. Nhận biết
- Nhận biết ion SO42- bằng ion Ba2+.
- Hiện tượng: Xuất hiện kết tủa trắng (BaSO4).
SƠ ĐỒ TƯ DUY
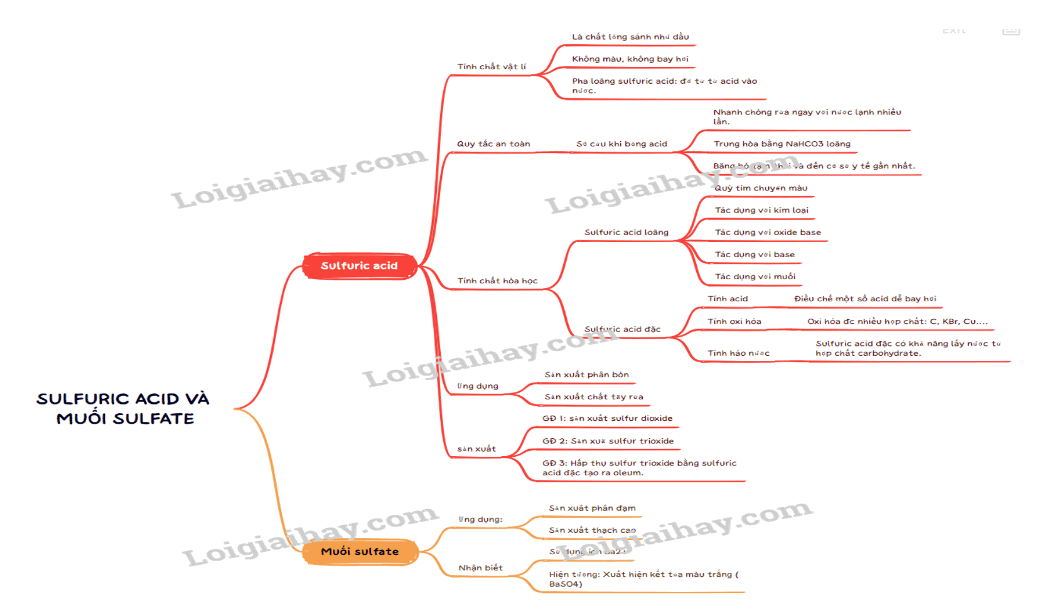
Luyện Bài Tập Trắc nghiệm Hóa lớp 11 - Kết nối tri thức - Xem ngay
Các bài khác cùng chuyên mục
- Lý thuyết Hợp chất hữu cơ và hóa học hữu cơ - Hóa học 11 Kết nối tri thức
- Bài 25. Ôn tập chương 6 trang 153, 154 Hóa học 11 Kết nối tri thức
- Bài 24. Carboxylic acid trang 145, 146, 147, 148, 149, 150, 151, 152 Hóa học 11 Kết nối tri thức
- Bài 23. Hợp chất carbonyl trang 136, 137, 138, 139, 140, 141, 142, 143, 144 Hóa học 11 Kết nối tri thức
- Bài 22. Ôn tập chương 5 trang 134, 135 Hóa học 11 Kết nối tri thức












Danh sách bình luận