Trắc nghiệm Bài 12. Phản ứng oxi hóa - khử và ứng dụng trong cuộc sống - Hóa 10 Chân trời sáng tạo
Đề bài
Số oxi hóa của nitơ trong NH4+ , NO2- , và HNO3 lần lượt là:
-
A.
+5, -3, +3.
-
B.
-3, +3, +5
-
C.
+3, -3, +5
-
D.
+3, +5, -3.
Số oxi hóa của Mn, Fe trong Fe3+ , S trong SO3 , P trong PO43-lần lượt là:
-
A.
0, +3, +6, +5
-
B.
0, +3, +5, +6
-
C.
+3, +5, 0, +6
-
D.
+5, +6, +3, 0.
Phản ứng nào là phản ứng oxi hoá - khử?
-
A.
2HgO \( \xrightarrow[]{t^{0}}\) 2Hg + O2
-
B.
СаСОз \( \xrightarrow[]{t^{0}}\) CaO + CO2.
-
C.
2Al(OH)3 \( \xrightarrow[]{t^{0}}\) Al2O3 + 3H2O
-
D.
2NaHCO3 \( \xrightarrow[]{t^{0}}\) Na2CO3 + CO2 + H2O
Ở phản ứng nào NH3 không đóng vai trò chất khử ?
-
A.
4NH3 + 5O2 \(\xrightarrow[{xt}]{{{t^0}}}\) 4NO + 6H2O
-
B.
2NH3 + 3Cl2 —> N2 + 6HCl
-
C.
NH3 + 3CuO \(\xrightarrow{{{t^0}}}\) 3Cu + N2 + 3H2O
-
D.
2NH3 + H2O2 + MnS04 —> Mn02 + (NH4)2SO4.
-
A.
Chỉ là chất oxi hoá.
-
B.
Chỉ là chất khử.
-
C.
Là chất oxi hoá, nhưng đồng thời cũng là chất khử.
-
D.
Không là chất oxi hoá, không là chất khử.
Phản ứng nào là phản ứng oxi hoá - khử?
-
A.
HNO3 + NaOH → NaNO3 + H2O
-
B.
N2O5+ H2O → 2HNO3
-
C.
2HNO3 + 3H2S → 3S + 2NO + 4H2O
-
D.
2Fe(OH)3 → Fe2O3 + 3H2O.
Cho sơ đồ phản ứng :
\(F{e_3}{O_4} + HN{O_3} \to Fe{\left( {N{O_3}} \right)_3} + NO + {H_2}O\)
Cân bằng PTHH của phản ứng trên. Các hệ số tương ứng với phân tử các chất là dãy số nào sau đây ?
-
A.
3, 14, 9, 1, 7
-
B.
3, 28, 9, 1, 14
-
C.
3, 26, 9, 2, 13
-
D.
2, 28, 6, 1, 14
Trong phản ứng đốt cháy \(CuFeS_2\) tạo ra sản phẩm \(CuO, Fe_2O_3\) và \(SO_2\) thì một phân tử \(CuFeS_2\) sẽ
-
A.
nhận 13e.
-
B.
nhận 12e.
-
C.
nhường 13e.
-
D.
nhường 12e.
Cho phản ứng : M2Ox + HN03 —> M(NO3)3 + ...
Khi x có giá trị là bao nhiêu thì phản ứng trên không thuộc loại phản ứng oxi hoá - khử ?
-
A.
x = 1
-
B.
x = 2
-
C.
x = 1 hoặc x = 2
-
D.
x = 3
Trong phản ứng: \(C{l_2} + {H_2}O \to HCl + HClO\), các nguyên tử Cl
-
A.
bị oxi hoá.
-
B.
bị khử.
-
C.
vừa bị oxi hoá, vừa bị khử.
-
D.
không bị oxi hoá, không bị khử.
Lời giải và đáp án
Số oxi hóa của nitơ trong NH4+ , NO2- , và HNO3 lần lượt là:
-
A.
+5, -3, +3.
-
B.
-3, +3, +5
-
C.
+3, -3, +5
-
D.
+3, +5, -3.
Đáp án : B
Trong hầu hết các hợp chất lấy
H có hóa trị I => số oxi hóa là +1
O có hóa trị II => số oxi hóa là -2
Tất cả các kim loại kiềm, kiềm thổ có hóa trị ứng với số nhóm trong bảng tuần hoàn => có số oxi hóa + 1; + 2
Nguyên tử luôn trung hòa về điện => tổng số oxi hóa của các chất trong phân tử = 0 => từ đó tính được số oxi hóa của các chất chưa biết.
Gọi số oxi hóa của N trong các hợp chất là x
Ta có: NH4+: x + 4 = 1 \( \to\) x = -3 \( \to\) số oxi hóa của N trong NH4+ là -3
NO2-: x + 2.(-2) = -1 \( \to\) x = 3 \( \to\) số oxi hóa của N trong NO2- là +3
HNO3: 1 + x + 3.(-2) = 0 \( \to\) x = 5 \( \to\) số oxi hóa của N trong HNO3 là +5
Số oxi hóa của Mn, Fe trong Fe3+ , S trong SO3 , P trong PO43-lần lượt là:
-
A.
0, +3, +6, +5
-
B.
0, +3, +5, +6
-
C.
+3, +5, 0, +6
-
D.
+5, +6, +3, 0.
Đáp án : A
Trong hầu hết các hợp chất lấy
H có hóa trị I => số oxi hóa là +1
O có hóa trị II => số oxi hóa là -2
Tất cả các kim loại kiềm, kiềm thổ có hóa trị ứng với số nhóm trong bảng tuần hoàn => có số oxi hóa + 1; + 2
Nguyên tử luôn trung hòa về điện => tổng số oxi hóa của các chất trong phân tử = 0 => từ đó tính được số oxi hóa của các chất chưa biết.
Mn là đơn chất nên có số oxi hóa 0
Fe3+ có số oxi hóa +3
SO3: x + 3.(-2) = 0 \( \to\) x = 6 \( \to\) số oxi hóa của S là +6
PO43-: x + 4.(-2) = -3 \( \to\) x = 5 \( \to\) số oxi hóa của P là +5
Phản ứng nào là phản ứng oxi hoá - khử?
-
A.
2HgO \( \xrightarrow[]{t^{0}}\) 2Hg + O2
-
B.
СаСОз \( \xrightarrow[]{t^{0}}\) CaO + CO2.
-
C.
2Al(OH)3 \( \xrightarrow[]{t^{0}}\) Al2O3 + 3H2O
-
D.
2NaHCO3 \( \xrightarrow[]{t^{0}}\) Na2CO3 + CO2 + H2O
Đáp án : A
Phản ứng oxi hóa khử là phản ứng hóa học trong đó đồng thời xảy ra sự oxi hóa và sự khử. Tức số oxi hóa của các chất trước và sau phản ứng thay đổi.
Những phản ứng theo đề bài cho, phản ứng oxi hóa khử là
\(2HgO\xrightarrow{{{t^0}}}2Hg + {O_2}\)
Hg2+ + 2e \( \to\) Hg0
2O2- \( \to\) O2 + 4e
Còn các phản ứng khác không phải là phản ứng oxi hóa khử
Ở phản ứng nào NH3 không đóng vai trò chất khử ?
-
A.
4NH3 + 5O2 \(\xrightarrow[{xt}]{{{t^0}}}\) 4NO + 6H2O
-
B.
2NH3 + 3Cl2 —> N2 + 6HCl
-
C.
NH3 + 3CuO \(\xrightarrow{{{t^0}}}\) 3Cu + N2 + 3H2O
-
D.
2NH3 + H2O2 + MnS04 —> Mn02 + (NH4)2SO4.
Đáp án : D
NH3 đóng vai trò là chất khử khi số oxi hóa của NH3 tăng sau phản ứng => các phản ứng còn lại NH3 sẽ đóng vai trò là chất oxi hóa
A,B,C số oxi hóa của NH3 đều tăng sau phản ứng => đóng vai trò là chất khử
=> ở phản ứng D NH3 đóng vai trò là môi trường
-
A.
Chỉ là chất oxi hoá.
-
B.
Chỉ là chất khử.
-
C.
Là chất oxi hoá, nhưng đồng thời cũng là chất khử.
-
D.
Không là chất oxi hoá, không là chất khử.
Đáp án : C
Chất oxi hóa là chất nhận e (tham gia quá trình khử)
Chất khử là chất cho e (tham gia quá trình oxi hóa)
NO2 đóng vai trò vừa là chất oxi hoá vừa là chất khử
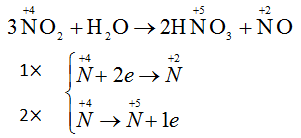
Quá trình 1 là quá trình khử
Quá trình 2 là quá trình oxi hóa
Phản ứng nào là phản ứng oxi hoá - khử?
-
A.
HNO3 + NaOH → NaNO3 + H2O
-
B.
N2O5+ H2O → 2HNO3
-
C.
2HNO3 + 3H2S → 3S + 2NO + 4H2O
-
D.
2Fe(OH)3 → Fe2O3 + 3H2O.
Đáp án : C
Phản ứng oxi hóa khử là phản ứng hóa học trong đó đồng thời xảy ra sự oxi hóa và sự khử( tức các chất có sự thay đổi số oxi hóa trước và sau phản ứng) => tìm ra được phản ứng oxi hóa khử.
Trong các phản ứng trên chi có phản ứng C là phản ứng oxi hoá - khử vì có sự thay đổi số oxi hoá của các nguyên tố.
![]()
Cho sơ đồ phản ứng :
\(F{e_3}{O_4} + HN{O_3} \to Fe{\left( {N{O_3}} \right)_3} + NO + {H_2}O\)
Cân bằng PTHH của phản ứng trên. Các hệ số tương ứng với phân tử các chất là dãy số nào sau đây ?
-
A.
3, 14, 9, 1, 7
-
B.
3, 28, 9, 1, 14
-
C.
3, 26, 9, 2, 13
-
D.
2, 28, 6, 1, 14
Đáp án : B
Cân bằng PTHH theo phương pháp thăng bằng electron
\(3F{e_3}{O_4} + 28HN{O_3} \to 9Fe{\left( {N{O_3}} \right)_3} + NO + 14{H_2}O\)
Trong phản ứng đốt cháy \(CuFeS_2\) tạo ra sản phẩm \(CuO, Fe_2O_3\) và \(SO_2\) thì một phân tử \(CuFeS_2\) sẽ
-
A.
nhận 13e.
-
B.
nhận 12e.
-
C.
nhường 13e.
-
D.
nhường 12e.
Đáp án : C
Viết quá trình oxi hóa của \(CuFeS_2\)
\(\mathop {CuFe{S_2}}\limits^0 \to \mathop {Cu}\limits^{ + 2} + \mathop {Fe}\limits^{ + 3} + 2\mathop S\limits^{ + 4} + 13e\)
=> 1 phân tử \(CuFeS_2\) nhường 13e
Cho phản ứng : M2Ox + HN03 —> M(NO3)3 + ...
Khi x có giá trị là bao nhiêu thì phản ứng trên không thuộc loại phản ứng oxi hoá - khử ?
-
A.
x = 1
-
B.
x = 2
-
C.
x = 1 hoặc x = 2
-
D.
x = 3
Đáp án : D
Để phản ứng không là phản ứng oxi hóa khử khi số oxi hóa của các nguyên tố trong phản ứng không thay đổi
Vì x = 3 thì số oxi hóa của M trước và sau phản ứng không thay đổi vẫn là +3
Trong phản ứng: \(C{l_2} + {H_2}O \to HCl + HClO\), các nguyên tử Cl
-
A.
bị oxi hoá.
-
B.
bị khử.
-
C.
vừa bị oxi hoá, vừa bị khử.
-
D.
không bị oxi hoá, không bị khử.
Đáp án : C
Xác định số oxi hóa của Cl trước và sau phản ứng
Số oxi hóa tăng => Chất khử, bị oxi hóa
Số oxi hóa giảm => Chất oxi hóa, bị khử
Ta có:
\({\mathop {Cl_2}\limits^0} + {H_2}O \to H\mathop {Cl}\limits^{ - 1} + H\mathop {Cl}\limits^{ + 1} O\)
Số oxi hóa của Cl vừa tăng, vừa giảm => Cl vừa bị oxi hoá, vừa bị khử.
- Trắc nghiệm Bài 18. Hydrogen halide và một số phản ứng của ion halide - Hóa 10 Chân trời sáng tạo
- Trắc nghiệm Bài 17. Tính chất vật lí và hóa học các đơn chất nhóm VIIA - Hóa 10 Chân trời sáng tạo
- Trắc nghiệm Bài 16. Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học - Hóa 10 Chân trời sáng tạo
- Trắc nghiệm Bài 15. Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng - Hóa 10 Chân trời sáng tạo
- Trắc nghiệm Bài 14. Tính biến thiên enthalpy của phản ứng hóa học - Hóa 10 Chân trời sáng tạo




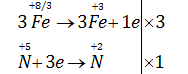






Danh sách bình luận