Lý thuyết bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Lý thuyết: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
I. Ảnh hưởng của nồng độ
- Ở nhiệt độ không đổi, tốc độ phản ứng tỉ lệ thuận với tích số nồng độ các chất phản ứng với số mũ thích hợp. Đối với phản ứng đơn giản (phản ứng chỉ xảy ra qua một giai đoạn), số mũ là hệ số của chất tham gia trong phương trình hóa học
- Giải thích: trong quá trình phản ứng, các hạt (phân tử, nguyên tử hoặc ion) luôn chuyển động không ngừng và va chạm với nhau. Những va chạm có năng lượng đủ lớn phá vỡ liên kết cũ và hình thành liên kết mới dẫn tới phản ứng hóa học.
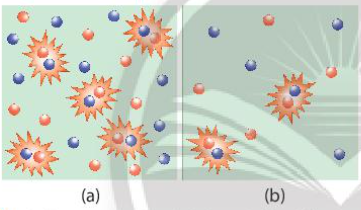
II. Ảnh hưởng của nhiệt độ
- Khi tăng nhiệt độ, tốc độ phản ứng tăng
- Giải thích: Ở nhiệt độ thường, các chất phản ứng chuyển động với tốc độ nhỏ, khi tăng nhiệt độ, các chất sẽ chuyển động với tốc độ lớn hơn, dẫn đến tăng số va chạm hiệu quả nên tốc độ phản ứng tăng
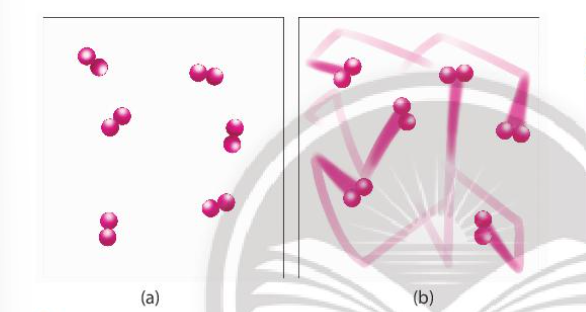
-Mối quan hệ giữa nhiệt độ và tốc độ phản ứng hóa học: \(\frac{{{v_2}}}{{{v_1}}} = {\gamma ^{\frac{{{T_2} - {T_1}}}{{10}}}}\)
Trong đó: v1, v2 là tốc độ phản ứng ở 2 nhiệt độ t1 và t2, γ là hệ số nhiệt độ Van’t Hoff
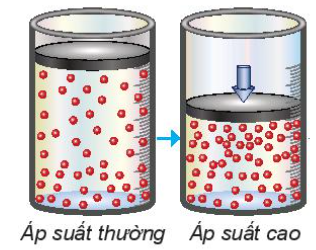
III. Ảnh hưởng của áp suất
- Việc tăng áp suất hỗn hợp khí cũng tương tự như tăng nồng độ, sẽ làm tốc độ phản ứng tăng
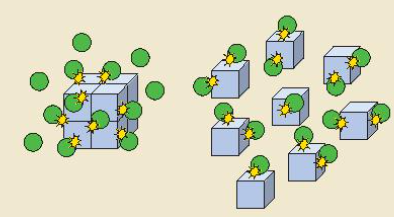
IV. Ảnh hưởng của bề mặt tiếp xúc
- Khi tăng diện tích bề mặt tiếp xúc, số va chạm giữa các chất đầu tăng lên, số va chạm hiệu quả cũng tăng theo, dẫn đến tốc độ phản ứng tăng
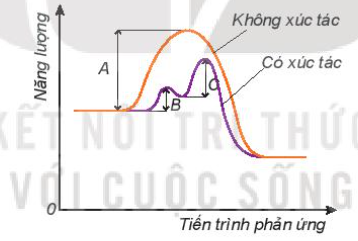
V. Ảnh hưởng của chất xúc tác
- Với một số phản ứng hóa học, để tăng tốc độ phản ứng, người ta sử dụng chất xúc tác, được ghi trên mũi tên trong phương trình hóa học
- Chất xúc tác làm tăng tốc độ của phản ứng hóa học, nhưng vẫn được bảo toàn về chất và lượng khi kết thúc phản ứng
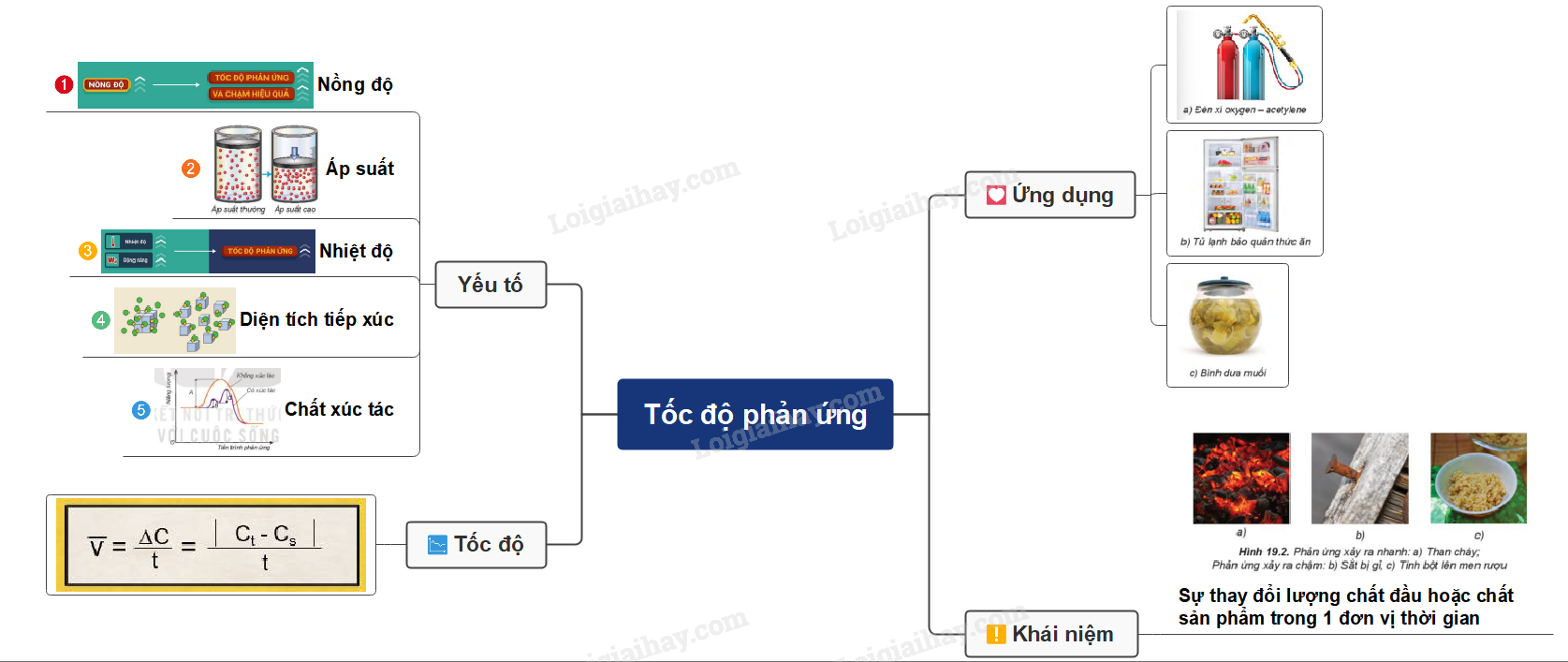
VI. Ý nghĩa thực tiễn của tốc độ phản ứng trong đời sống và sản xuất
- Trong đời sống và trong sản xuất, con người áp dụng nhiều biện pháp kĩ thuật để thay đổi tốc độ phản ứng như thay đổi nồng độ, nhiệt độ, chất xúc tác…

Luyện Bài Tập Trắc nghiệm Hóa 10 - Chân trời sáng tạo - Xem ngay
Các bài khác cùng chuyên mục
- Lý thuyết bài 18: Hydrogen halide và một số phản ứng của ion Halide
- Lý thuyết bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
- Lý thuyết bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
- Lý thuyết bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
- Lý thuyết bài 14: Tính biến thiên enthalpy của phản ứng hóa học












Danh sách bình luận