Câu hỏi
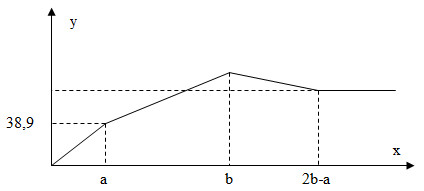
Cho từ từ đến dư dung dịch H2SO4 vào dung dịch chứa NaAlO2 và BaCl2. Khối lượng kết tủa (y gam) phụ thuộc vào số mol H2SO4 (x mol) theo đồ thị như hình vẽ. Khối lượng kết tủa cực đại là
- A 108,8 gam.
- B 73,85 gam.
- C 58,25 gam.
- D 66,05 gam.
Phương pháp giải:
Xét 2 trường hợp:
TH1: Tại x = a thì BaSO4 đạt cực đại, Al(OH)3 chưa đạt cực đại
TH2: Tại x = a thì Al(OH)3 đạt cực đại, BaSO4 vẫn chưa đạt cực đại
Công thức tính nhanh:
nH+ = 4nAlO2- – 3nAl(OH)3
Lời giải chi tiết:
Các phản ứng:
Ba2+ + SO42- → BaSO4
H+ + AlO2- + H2O → Al(OH)3
3H+ + Al(OH)3 → Al3+ + 3H2O
TH1: Tại x = a thì BaSO4 đạt cực đại, Al(OH)3 chưa đạt cực đại
- Tại nH2SO4 = a (mol) thì BaSO4 đạt cực đại (Ba2+ bị kết tủa hoàn toàn dưới dạng BaSO4)
nBa2+ = nSO42- = nBaSO4 = a (mol) => mBaSO4 = 233a (g)
nH+ = nAl(OH)3 = 2a (mol) => mAl(OH)3 = 156a (g)
=> m ↓ = 233a + 156a = 38,9 => a = 0,1 mol
- Tại nH2SO4 = b (mol) thì Al(OH)3 đạt cực đại (AlO2- chuyển hết thành Al(OH)3)
nH+ = nAlO2- = nAl(OH)3max = 2b (mol)
- Tại nH2SO4 = 2b-a (mol) thì Al(OH)3 vừa bị hòa tan hết thành Al3+
=> nH+ = nAlO2- + 3nAl(OH)3 max = 4nAlO2- => 4b-2a = 4.2b => b < 0 loại
TH2: Tại x = a thì Al(OH)3 đạt cực đại, BaSO4 vẫn chưa đạt cực đại
- Tại nH2SO4 = a (mol) thì Al(OH)3 đạt cực đại, BaSO4 chưa đạt cực đại
nAl(OH)3 = nH+ = 2a mol => nAlO2 max = 2a mol
nBaSO4 = nSO42- = a mol
=> m ↓ = 78.2a + 233a = 38,9 => a = 0,1 mol
- Tại x = 2b – a thì Al(OH)3 bị hòa tan hoàn toàn:
=> nH+ = 4nAlO2- => 4b-2a = 4.2a => b = 0,25 mol
- Tại x = b thì BaSO4 cực đại, khối lượng của kết tủa lớn nhất
nBaSO4 max = nSO42- = b = 0,25 mol
mAl(OH)3 = (4nAlO2- - nH+)/3 = (4.0,2 – 0,5)/3 = 0,1 mol
=> m kết tủa cực đại = 0,25.233 + 0,1.78 = 66,05 gam
Đáp án D







