Câu hỏi
Cho 4 mol N2 và 16 mol H2 vào bình kín. Tại thời điểm cân bằng thu được x mol hỗn hợp khí. Biết hiệu suất của phản ứng tổng hợp NH3 là 70%. Tính x?
- A 14,1
- B 14,4
- C 14,3
- D 14,2
Phương pháp giải:
Phương pháp:
=> H tính theo N2
H= mol
N2 + 3 H2 <-> 2NH3
Thay vào PT tính số mol hỗn hợp sau phản ứng
Lời giải chi tiết:
Hướng dẫn giải
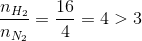
=> H tính theo N2
H= 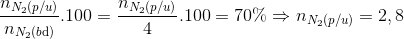 mol
mol
N2 + 3 H2 <-> 2NH3
bđ 4 16
p/u 2,8 8,4 5,6
sau 1,2 7,6 5,6
=> x=14,4 mol
Đáp án B.







