 Môn Hóa - Lớp 11
Môn Hóa - Lớp 11
 30 bài tập về xác định công thức phân tử dựa vào quá trình phân tích định lượng có lời giải
30 bài tập về xác định công thức phân tử dựa vào quá trình phân tích định lượng có lời giải
Câu hỏi
Đốt cháy hoàn toàn một hidrocacbon A thu được hỗn hợp X gồm CO2 và H2O.Dẫn toàn bộ hỗn hợp X vào trong bình đựng dung dịch Ba(OH)2 (dư) thu được 39,4 gam kết tủa đồng thời khối lượng bình tăng 12,4 gam.Vậy Acó thể là
- A C2H2.
- B C2H4.
- C C4H6.
- D C3H8
Phương pháp giải:
Bảo toàn nguyên tố : nC = nCO2 , nH = 2 nH2O
CxHy :
m tủa = m BaCO3 , nBaCO3 = n CO2 , m bình tăng = m CO2 + m H2O
Lời giải chi tiết:
Hướng dẫn Giải :
n BaCO3 = n CO2 = 0,2 mol => m CO2 = 8,8 g
=>m bình tăng = m CO2 + m H2O = 12.4
=>m H2O = 3.6 g => n H2O = 0.2 mol
=>n C = n CO2= 0.2 mol
=>n H = 2 n H2O = 0.4 mol
CxHy :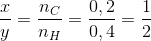
=>Công thức của hidrocacbon là C2H4
Đáp án B






