Câu hỏi
Cho m gam Cu vao dd chứa 0,04 mol AgNO3 một thời gian thu được dd Y và 3,88 g chất rắn X. Cho 2,925 g Zn vào dd Y đến phản ứng hoàn toàn thu được dd Z và 3,217 g chất rắn T. Tính m :
- A 1,216g
- B 1,088 g
- C 1,344g
- D 1,152g
Phương pháp giải:
Phương pháp :
Bảo toàn khối lượng
Bảo toàn điện tích
Lời giải chi tiết:
Hướng dẫn giải :
nZn =0,052 > nAgNO3 → dd Z chỉ chứa Zn(NO3)2
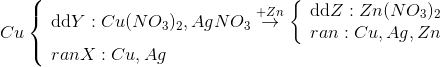
Bảo toàn số mol NO3 thì nZn(NO3)2(Z) =0,02 mol→ rắn T có mZn = 2,925-0,02.65=1,625g
Trong rắn T đặt nCu =x, nAg =y → 64x + 108y=3,217-1,625 = 1,592(g)
Bảo toàn điện tích trong dd Y có 2x + y =0,04 → x =0,018 mol y =0,004 mol
Bảo toàn khối lượng Cu và Ag trong phản ứng td với AgNO3 có
m + 0,04.108=mCu(Y) +mAg(Y) +3,88 → m =0,018.64+0,004.108+3,88-0,04.108=1,152 (g)
Đáp án D







