Câu hỏi
Dựa vào các thông tin được cung cấp dưới đây để trả lời các từ 91 đến 93
Sự điện phân là quá trình oxi hóa - khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân:
+ Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
Cho dãy điện hóa sau:
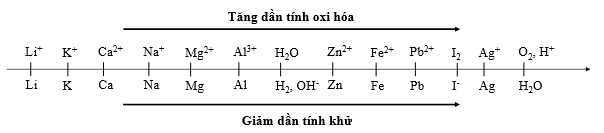
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời Pb(NO3)2 và Al(NO3)3 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân theo sơ đồ như hình bên.
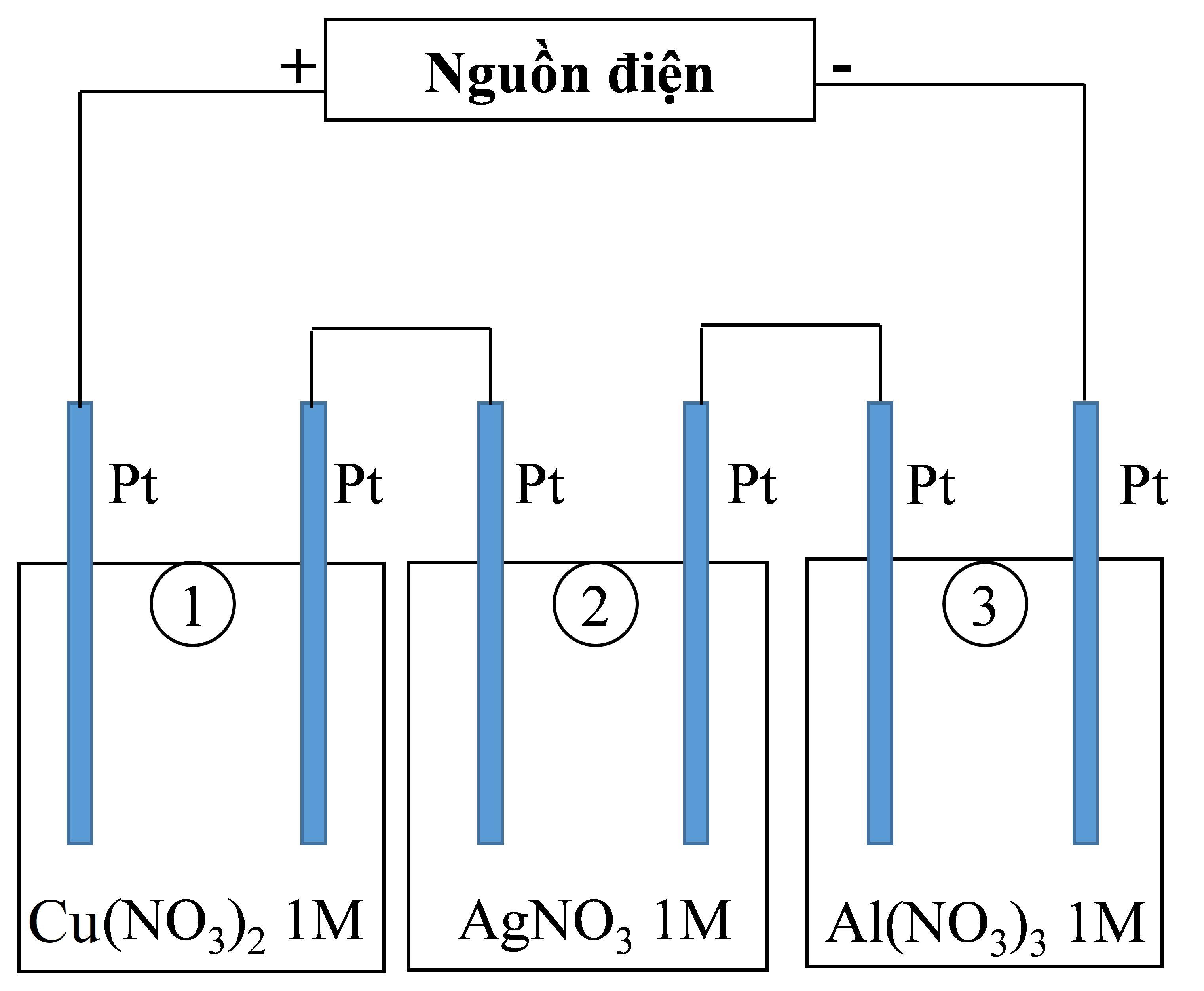
Sau một thời gian, sinh viên quan sát thấy có 3,84 gam kim loại đồng bám lên điệc cực của bình 1. Biết trong hệ điện phân nối tiếp, số điện tử truyền dẫn trong các bình là như nhau. Nguyên tử khối của Ag, Cu và Al lần lượt là 108; 64 và 27 đvC.
Câu 1:
Trong thí nghiệm 1, bán phản ứng nào xảy ra ở catot?
- A Pb2+ + 2e → Pb.
- B Al3+ + 3e → Al.
- C O2 + 4H+ + 4e → 2H2O.
- D H2O + 2e → H2 + 2OH-.
Phương pháp giải:
Catot của thiết bị là nơi xảy ra bán phản ứng khử.
Lời giải chi tiết:
Bán phản ứng xảy ra ở catot là Pb2+ + 2e → Pb.
Chú ý: Al3+ không bị điện phân.
Chọn A.
Câu 2:
Nếu trong thí nghiệm 1, người sinh viên đổi 2 điện cực than chì bằng 2 điện cực kim loại Pb, phản ứng nào xảy ra ở catot và anot?
- A Catot: Pb2+ + 2e → Pb; Anot: 2H2O → O2 + 4H+ + 4e.
- B Catot: Al3+ + 3e → Al; Anot: Pb → Pb2++ 2e.
- C Catot: 2H2O + 2e → H2 + 2OH-; Anot: Pb → Pb2+ + 2e.
- D Catot: Pb2+ + 2e → Pb; Anot: Pb → Pb2+ + 2e.
Phương pháp giải:
- Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa; catot của thiết bị là nơi xảy ra bán phản ứng khử.
- Khi điện phân dung dịch sử dụng kim loại làm cực dương trùng với ion kim loại bị điện phân thì sẽ xảy ra hiện tượng dương cực tan.
Lời giải chi tiết:
Tại catot xảy ra bán phản ứng: Pb2+ + 2e → Pb
Tại anot xảy ra bán phản ứng: Pb → Pb2+ + 2e (cực dương tan dần nên được gọi là hiện tượng dương cực tan).
Chọn D.
Câu 3:
Trong thí nghiệm 2, số gam kim loại Ag bám lên điện cực trong bình 2 là
- A 0 gam.
- B 3,24 gam.
- C 12,96 gam.
- D 6,48 gam.
Phương pháp giải:
Điện phân dung dịch có thể điều chế các kim loại hoạt động trung bình hoặc yếu (các kim loại đứng sau Al trong dãy điện hóa) bằng cách điện phân dung dịch muối của chúng.
Lời giải chi tiết:
Điện phân dung dịch có thể điều chế các kim loại hoạt động trung bình hoặc yếu (các kim loại đứng sau Al trong dãy điện hóa) bằng cách điện phân dung dịch muối của chúng.
→ Cu2+ và Ag+ bị điện phân; Al3+ không bị điện phân.
Catot của bình 1 (-): Cu2+ + 2e → Cu
⟹ ne trao đổi (1) = 2.nCu = 2.\(\frac{{3,84}}{{64}}\) = 0,12 mol
Catot của bình 2 (-): Ag+ + 1e → Ag
⟹ ne trao đổi (1) = nAg
Do 3 bình điện phân mắc nối tiếp nên mol electron trao đổi như nhau
⟹ ne trao đổi (1) = ne trao đổi (2) ⟹ nAg = 0,12 mol
Khối lượng Ag bám lên điện cực trong bình 2 là: mAg = 0,12.108 = 12,96 gam.
Chọn C.







