Câu hỏi
Hoà tan hoàn toàn 16 gam hỗn hợp Mg và Fe bằng dung dịch H2SO4 loãng 20% (vừa đủ). Sau phản ứng thấy khối lượng dung dịch tăng thêm 15,2 gam. Nồng độ % của MgSO4 có trong dung dịch sau phản ứng là
- A 19,76%.
- B 11,36%.
- C 15,74%.
- D 9,84%.
Phương pháp giải:
Nhận xét: mdd tăng = mKL – mH2 → tìm được m và n của H2
Giải hệ phương trình với ẩn là số mol của Mg và Fe ta được số mol từng kim loại → tìm số mol MgSO4
- Tính số mol H2SO4 → mdd ban đầu → mdd sau → C%
Lời giải chi tiết:
mdd tăng = mKL – mH2
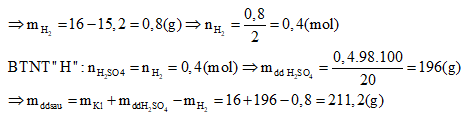
Đặt nMg = x và nFe = y, ta có:
\(\left\{ \begin{array}{l}{m_{hh}} = 24x + 56y = 16\\x + y = {n_{{H_2}}} = 0,4\end{array} \right. \Rightarrow \left\{ \begin{array}{l}x = 0,2 = {n_{MgS{O_4}}}\\y = 0,2\end{array} \right.\)
\(C{\% _{MgS{O_4}}} = \frac{{{m_{MgS{O_4}}}}}{{{m_{dd\,sau}}}}.100\% = \frac{{0,2.120}}{{211,2}}.100\% = 11,36\% \)
Đáp án B







