Câu hỏi
Cho phương trình phản ứng:
Al + HNO3 loãng → Al(NO3)3 + N2 + H2O
a) Xác định vai trò của từng chất tham gia phản ứng và nêu sự oxi hóa, sự khử.
b) Cân bằng phản ứng trên theo phương pháp thăng bằng electron.
Phương pháp giải:
a) Chất khử là chất nhường electron (số oxi hóa tăng)
Chất oxi hóa là chất nhận electron (số oxi hóa giảm)
Quá trình khử là quá trình nhận electron
Quá trình oxi hóa là quá trình nhường electron
b) Các bước cân bằng phản ứng oxi hóa - khử theo phương pháp thăng bằng electron:
- Xác định số oxi hóa của các nguyên tố để tìm chất oxi hoá (có số oxi hóa giảm) và chất khử (có số oxi hóa tăng).
- Viết quá trình oxi hóa và quá trình khử, cân bằng mỗi quá trình.
- Tìm hệ số thích hợp cho chất oxi hóa và chất khử sao cho tổng số electron cho bằng tổng số electron nhận.
- Đặt hệ số của các chất oxi hóa và chất khử vào sơ đồ phản ứng, từ đó tính ra hệ số các chất khác.
Lời giải chi tiết:
a) Xác định vai trò của từng chất tham gia phản ứng và nêu sự oxi hóa, sự khử:
\(\mathop {Al{\rm{ }}}\limits^0 + {\rm{ }}H\mathop N\limits^{ + 5} {O_3}{\,_{loang}}{\rm{ }} \to {\rm{ }}\mathop {Al}\limits^{ + 3} {\left( {N{O_3}} \right)_3} + {\rm{ }}{\mathop N\limits^0 _2} + {\rm{ }}{H_2}O\)
- Số oxi hóa của Al tăng từ 0 lên +3 => Al là chất khử
- Số oxi hóa của N giảm từ +5 xuống 0 => HNO3 là chất oxi hóa
- Sự oxi hóa: Al → Al+3 + 3e
- Sự khử: 2N+5 + 10e → N2
b) Cân bằng phản ứng trên theo phương pháp thăng bằng electron.
\(\mathop {Al{\rm{ }}}\limits^0 + {\rm{ }}H\mathop N\limits^{ + 5} {O_3}{\,_{loang}}{\rm{ }} \to {\rm{ }}\mathop {Al}\limits^{ + 3} {\left( {N{O_3}} \right)_3} + {\rm{ }}{\mathop N\limits^0 _2} + {\rm{ }}{H_2}O\)
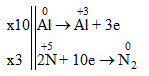
10Al + 36HNO3 loãng → 10Al(NO3)3 + 3N2 +18 H2O







