Câu hỏi
Vị trí các nguyên tố X, Y, R, T trong bảng tuần hoàn như sau:
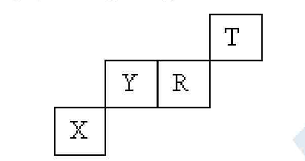
X có cấu hình electron lớp ngoài cùng là 4s24p2. Tổng số proton của 3 nguyên tử X, R, T là:
- A 56
- B 57
- C 40
- D 64
Phương pháp giải:
Dựa vào vị trí của X, Y, R, T để tìm cấu hình electron của các nguyên tử. Từ đó xác định được tổng số proton của 3 nguyên tử X, R, T.
Lời giải chi tiết:
Vì X có cấu hình electron lớp ngoài cùng là 4s24p2 nên cấu hình electron đầy đủ của X là 1s22s22p63s23p63d104s24p2. Vậy nguyên tử X có 32 electron, 32 proton. Nguyên tố X thuộc nhóm IVA.
Gọi nguyên tố Z là nguyên tố cùng nhóm với X và đứng ngay trước nguyên tố Y.
Vì X và Z thuộc cùng nhóm và nằm ở 2 chu kì liên tiếp nên xét các trường hợp:
TH1: nguyên tố Z có 32- 8= 24 electron.
Cấu hình electron nguyên tử của Z là 1s22s22p63s23p63d54s1. Nguyên tố Z thuộc nhóm VIB.
Vậy trường hợp này loại.
TH2: nguyên tố Z có 32- 18 = 14 electron.
Cấu hình electron nguyên tử của Z là 1s22s22p63s23p2. Nguyên tố Z thuộc nhóm IVA.
Vậy trường hợp 2 thỏa mãn.
Nguyên tố Z đứng ngay trước nguyên tố Y nên Y có số hiệu nguyên tử là 14 + 1= 15
Suy ra số proton của nguyên tử Y bằng 15.
Nguyên tố Y đứng ngay trước nguyên tố R nên R có số hiệu nguyên tử là 15 + 1= 16
Suy ra số proton của nguyên tử R bằng 16.
Gọi Q là nguyên tố thuộc cùng nhóm với nguyên tố R và đứng trước nguyên tố T
Suy ra số hiệu nguyên tử Q bằng 16 – 8= 8 và số hiệu nguyên tử nguyên tố T là 8 + 1= 9
Tổng số proton của 3 nguyên tử X, R, T là: 32 + 16 + 9= 57
Đáp án B







