Lý thuyết Phương trình trạng thái khí lí tưởng - Vật lí 12 Cánh diều
Mối liên hệ giữa thể tích và áp suất của chất khí Mối liên hệ giữa thể tích và nhiệt độ của chất khí Phương trình trạng thái khí lí tưởng
Bài 2. Phương trình trạng thái khí lí tưởng
I. Mối liên hệ giữa thể tích và áp suất của chất khí
Định luật Boyle
- Với một khối lượng khí xác định, khi giữ nhiệt độ của khí không đổi thì áp suất gây ra bởi khí tỉ lệ nghịch với thể tích của nó
pV = hằng số
- Đồ thị biểu diễn định luật Boyle là một nhánh của đường hypebol.
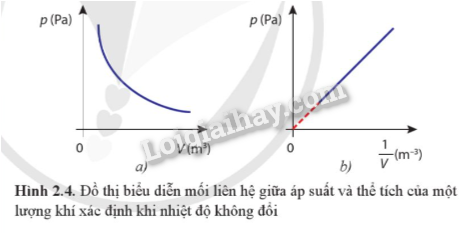
- Công thức còn viết dưới dạng
\({p_1}{V_1} = {p_2}{V_2}\)
II. Mối liên hệ giữa thể tích và nhiệt độ của chất khí
Định luật Charles
- Với một khối lượng khí xác định, khi giữ áp suất không đổi thì thể tích của khí tỉ lệ thuận với nhiệt độ tuyệt đối của nó
\(\frac{V}{T} = \) hằng số
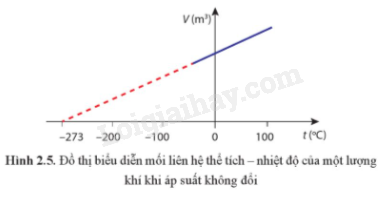
III. Phương trình trạng thái khí lí tưởng
\(pV = nRT\)
Hay \(\frac{{{p_1}{V_1}}}{{{T_1}}} = \frac{{{p_2}{V_2}}}{{{T_2}}}\)
Trong đó:
\(n = \frac{m}{M}\) là số mol của khối khí
\(R \approx 8,31\,\,\frac{J}{{mol.K}}\) là hằng số, gọi là hằng số khí lí tưởng
Quá trình chuyển trạng thái không phụ thuộc cách chuyển trạng thái mà chỉ phụ thuộc trạng thái đầu và trạng thái cuối.
Sơ đồ tư duy về “Phương trình trạng thái khí lí tưởng”
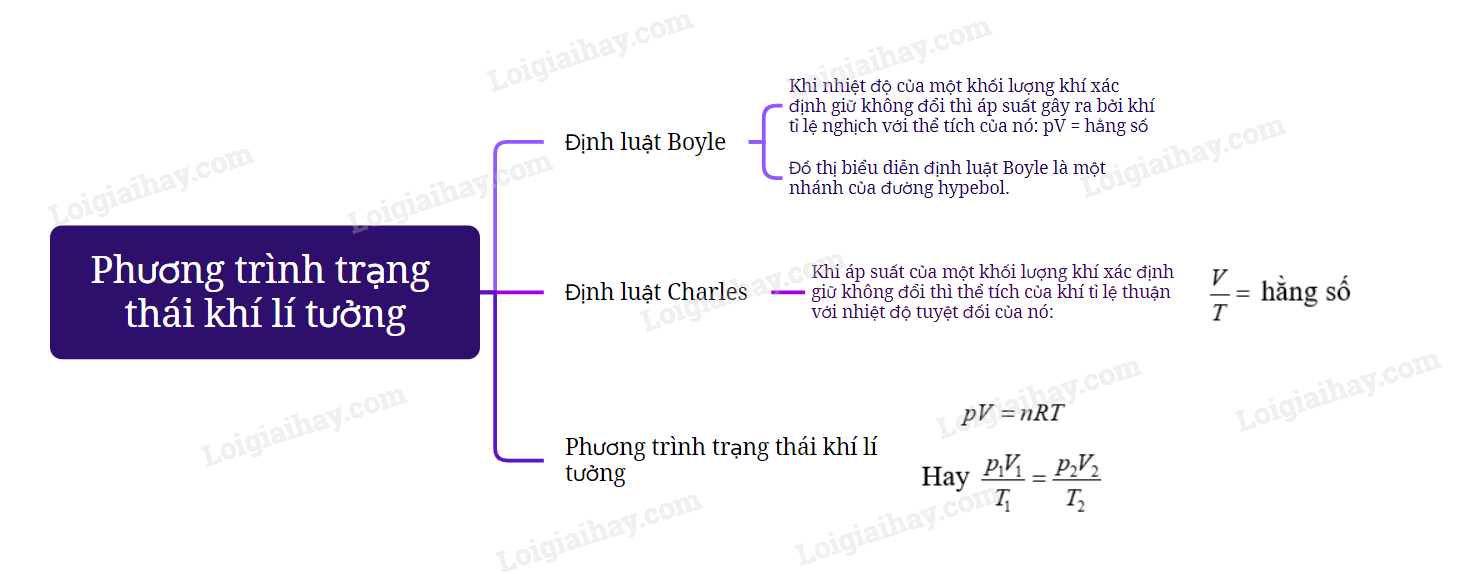












Danh sách bình luận