Lý thuyết Nguyên tố nhóm IA - Hóa 12 Kết nối tri thức
Nguyên tố nhóm IA là những nguyên tố s
I. Đơn chất nhóm IA
1. Đặc điểm chung
- Nguyên tố nhóm IA là những nguyên tố s, chỉ có 1electron hóa trị ở phân lớp ns1 và đứng đầu mỗi chu kì tương ứng. Kim loai IA có thế điện cực chuẩn \(E_{{M^ + }/M}^o\)rất nhỏ, nên dễ tách electron hóa trị ra khỏi ngyên tử. Vì vậy, trong các phản ứng hóa học, chúng dễ nhường 1 electron, thể hiện tính khử rất mạnh
- Trong hợp chất, nguyên tử kim loại nhóm IA chỉ thể hiện số oxi hóa +1
2. Trạng thái tự nhiên
Trong tự nhiên, các nguyên tố nhóm IA chỉ tồn tại ở dạng hợp chất (chủ yếu là dạng muối). Sodium và potassium là hai nguyên tố phổ biến trong vỏ Trái Đất, có nhiều trong nước biển, mỏ muối, quặng halite (NaCl), quặng sylvinite (NaCl.KCl)
3. Tính chất vật lí
a) Nhiệt độ nóng chảy và nhiệt độ sôi
- Trong nhóm IA, nhiệt độ nóng chảy và nhiệt độ sôi của các kim loại có xu hướng giảm dần từ Li đến Cs
- Các kim loại nhosm IA đều dễ nóng chảy và có nhiệt độ nóng chảy thấp hơn so với các kim loại nhóm khác.
b) Khối lượng riêng
Các kim loại nhóm IA có khối lượng riêng nhỏ (đều là kim loại nhẹ) do có bán kính nguyên tử lớn và cấu trúc tính thể kém đặc khít
c) Độ cứng
Do có liên kết kim loại yếu nên các kim loại nhóm IA có độ cứng thấp (đều mềm, có thể cắt bằng dao, kéo)
4. Tính chất hóa học
- Kim loại kiềm là những kim loại hoạt động hóa học mạnh, có tính khử mạnh và tính khử tăng dần từ Li đến Cs
- Các kim loại kiềm có thế điện cực chuẩn rất âm, do đó chúng đều phản ứng với nước ở điều kiện thường với mức độ tăng dần từ Li đến Cs.
5. Bảo quản
Các kim loại nhóm IA được bảo quản trong dầu hỏa, trong chân không hoặc trong khí hiếm.
II. Hợp chất của kim loại nhóm IA
1. Đặc điểm chung
- Các hợp chất của kim loại kiềm thường dễ tan trong nước và tạo thành dung dịch chất điện li mạnh
- Ở điều kiện thường, các ion kim loại nhóm IA đều không có màu. Tuy nhiên, đốt nóng kim loại kiềm hoặc các hợp chất của chúng trên ngọn lửa không màu làm ngọn lửa có màu đặc trưng. Do vậy, có thể nhận biết hợp chất của kim loại nhóm IA bằng màu ngọn lửa.
2. Hợp chất quan trọng
a) Sodium chloride
- Ứng dụng:

- Quá trình điện phân dung dịch NaCl:
Trong công nghiệp chlorine – kiềm, quá trình điện phân dung dịch NaCl bão hòa có màng ngăn điện cực được ứng dụng để sản xuất xút công nghiệp (NaOH), khí chlorine (Cl2). Điện phân dung dịch NaCl bão hòa không có màng ngăn điện cực được ứng dụng để sản xuất nước Javel (NaClO)
b) Sodium hydrogencarbonate, sodium carbonate
- Ứng dụng
- NaHCO3 có dạng bột, màu trắng, còn được gọi là baking soda
Trong sản xuất và đời sống, baking soda có một số ứng dụng như
+ Điều chỉnh vị chua của nước giải khát theo phản ứng
+ Làm tăng độ xốp của bánh, làm mềm thực phẩm. Đó là do sau khi trộn baking soda vào bột làm bánh hoặc tẩm ướp baking soda vào thực phẩm và đun nóng, NaHCO3 bị phân hủy sinh ra khí CO2, hơi nước
- Sodium carbonate

- Sản xuất
Trong công nghiệp, sodium hydrogencarbonate (baking soda) và sodium carbonate (soda) được sản xuất bằng phương pháp Solvay từ nguyên liệu chính là đá vôi, muối ăn, ammonia và nước
Quá trình Solvay sản xuất soda gồm hai giai đoạn chính
+ Giai đoạn tạo NaHCO3: NaCl + NH3 + CO2 + H2O \( \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} \)NaHCO3 + NH4Cl
Khi làm lạnh NaHCO3 kết tinh và được lọc, tách khỏi hệ phản ứng.
+ Giai đoạn tạo Na2CO3: 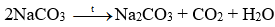
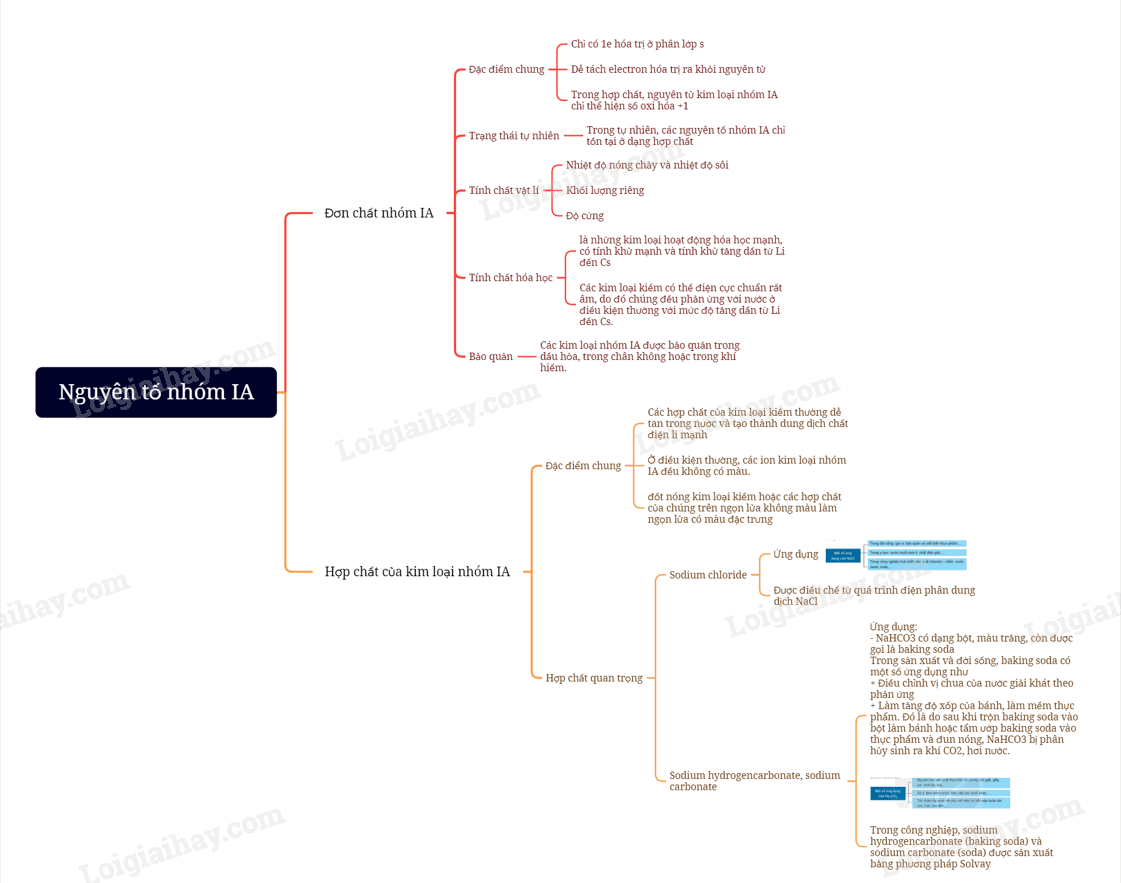
SƠ ĐỒ TƯ DUY
Luyện Bài Tập Trắc nghiệm Hóa 12 - Kết nối tri thức - Xem ngay
Các bài khác cùng chuyên mục
- Lý thuyết Một số tính chất và ứng dụng của phức chất - Hóa 12 Kết nối tri thức
- Lý thuyết Sơ lược về phức chất - Hóa 12 Kết nối tri thức
- Lý thuyết Đại cương về kim loại chuyển tiếp dãy thứ nhất - Hóa 12 Kết nối tri thức
- Lý thuyết Nguyên tố nhóm IIA - Hóa 12 Kết nối tri thức
- Lý thuyết Nguyên tố nhóm IA - Hóa 12 Kết nối tri thức












Danh sách bình luận