Câu hỏi
Thổi một luồng CO qua hỗn hợp Fe và Fe2O3 nung nóng được chất khí B và hỗn hợp D gồm Fe, FeO, Fe2O3, Fe3O4. Cho B lội qua dung dịch nước vôi trong dư thấy tạo ra 6 gam kết tủa. Hòa tan D bằng H2SO4 đặc, nóng thấy tạo ra 0,18 mol SO2 còn dung dịch E. Cô cạn E thu được 24 gam muối khan. Thành phần phần trăm khối lượng của Fe trong hỗn hợp đầu là
- A 58,33%.
- B 50%.
- C 41,67%.
- D 40%.
Phương pháp giải:
Đặt x và y lần lượt là số mol của Fe và Fe2O3 trong hỗn hợp ban đầu
Sau tất cả quá trình Fe từ 0 lên +3 ; C từ +2 lên C +4 ; S từ +6 xuống S +4 nên ta có
BTNT "Fe": nFe ban đầu = 2nFe2(SO4)3 = 2.0,06 = 0,12 (mol)
=> x + 2y = 0,12 (1)
BTNT "C": nCO = nCaCO3 = 0,06 (mol)
Qúa trình nhường e
Fe → Fe+3 + 3e
x → 3x (mol)
C+2 → C +4 +2e
0,06 → 0,12 (mol)
Qúa trình nhận e
S+6 + 2e → S+4
0,36← 0,18(mol)
∑ ne (nhường) = ∑ ne (nhận) => x =? (mol)
Từ (1) => y = ? (mol)
Có x, y từ đó dễ dàng tính được % mFe
Lời giải chi tiết:
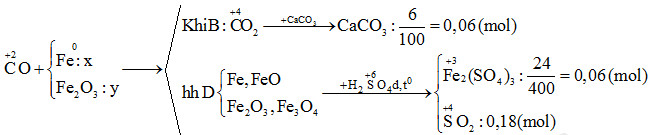
Đặt x và y lần lượt là số mol của Fe và Fe2O3 trong hỗn hợp ban đầu
Sau tất cả quá trình Fe từ 0 lên +3 ; C từ +2 lên C +4 ; S từ +6 xuống S +4 nên ta có
BTNT "Fe": nFe ban đầu = 2nFe2(SO4)3 = 2.0,06 = 0,12 (mol)
=> x + 2y = 0,12 (1)
BTNT "C": nCO = nCaCO3 = 0,06 (mol)
Qúa trình nhường e
Fe → Fe+3 + 3e
x → 3x (mol)
C+2 → C +4 +2e
0,06 → 0,12 (mol)
Qúa trình nhận e
S+6 + 2e → S+4
0,36← 0,18(mol)
∑ ne (nhường) = ∑ ne (nhận)
=> 3x + 0,12 = 0,36
=> x = 0,08 (mol)
Từ (1) => y = 0,02 (mol)
\(\% mFe = {{{m_{Fe}}} \over {{m_{hh}}}}.100\% = {{0,08.56} \over {0,08.56 + 0,02.160}}.100\% = 58,33\% \)
Đáp án A







