Câu hỏi
Điện phân dung dịch chứa đồng thời NaCl và CuSO4 (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan các khí trong nước và sự bay hơi nước) với cường độ dòng điện không đổi. Kết quả của thí nghiệm ghi ở bảng sau
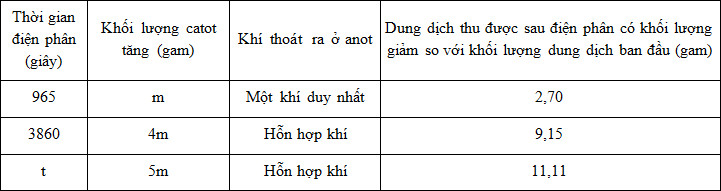
Giá trị của t là
- A 4101.
- B 5790.
- C 9650.
- D 11580.
Lời giải chi tiết:
* t1 = 965 giây => ne = It/F = 965.I/96500 = 0,01.I (mol)
Do sau thời điểm t = 965 giây lượng kim loại bám vào catot vẫn tiếp tục tăng nên t = 965 giây thì kim loại chưa bị điện phân hết.
Anot thu được khí duy nhất là Cl2 => nCl2 = 0,5ne = 0,005I (mol)
=> m dd giảm = m + 0,005I.71 = 2,7 (1)
nCu = m/64 (g) => ne = 2nCu = m/32 (mol) => m/32 = 0,01.I (2)
Giải (1) và (2) thu được m = 1,28 và I = 4
* t2 = 3860 giây = 4t1
Sau t2 = 3860 giây lượng kim loại vẫn tiếp tục tăng nên tại t2 = 3860 giây thì KL chưa bị điện phân hết.
ne(t2) = 3860.4/96500 = 0,16 mol
Đặt số mol khí Cl2 và O2 ở anot lần lượt là x và y (mol)
+ m dd giảm = mCl2 + mO2 + mCu => 71x + 32y + 4.1,28 = 9,15 (3)
+ BT e: 2nCl2 + 4nO2 = n e => 2x + 4y = 0,16 (4)
Giải (3) và (4) thu được x = 0,05 và y = 0,015
=> nNaCl = 2nCl2 = 0,1 mol
*t3 = t giây:
TH1: Cu2+ chưa bị điện phân hết
n e (catot) = 2.nCu = 2.5.1,28/64 = 0,2 mol
Ta có: m dd giảm = mCl2 + mO2 + mCu => 11,11 = 0,05.71 + mO2 + 5.1,28 => mO2 = 1,16 gam
=> nO2 = 0,03625 mol
=> n e (anot) = 2nCl2 + 4nO2 = 0,245 mol
Ta thấy: n e (catot) ≠ n e (anot) (loại)
TH2: Cu2+ bị điện phân hết, H2O đã bị điện phân
Đặt số mol H2 sinh ra ở catot là a và số mol O2 sinh ra ở anot là b (mol)
+ n e (catot) = 2nCu + 2nH2 = 2.5.1,28/64 + 2a = 2a + 0,2 (mol)
n e (anot) = 2nCl2 + 4nO2 = 2.0,05 + 4b = 4b + 0,1 (mol)
BTe cho 2 điện cực: 2a + 0,2 = 4b + 0,1 (*)
+ m dd giảm = mCl2 + mO2 + mCu + mH2 => 0,05.71 + 32b + 5.1,28 + 2a = 11,11 (**)
Giải hệ thu được a = 0,02 và b = 0,035
=> n e = 2a + 0,2 = 0,24 mol
=> t = ne.F/I = 0,24.96500/4 = 5790 giây
Đáp án B







