Câu hỏi
Hòa tan hoàn toàn 9,8 gam hỗn hợp X gồm Na và Al2O3 vào nước thu được 1,792 lít H2 (đktc) và dung dịch Y. Cho từ từ dung dịch HCl vào dung dịch Y thì thấy khối lượng kết tủa biến thiên theo đồ thị sau:
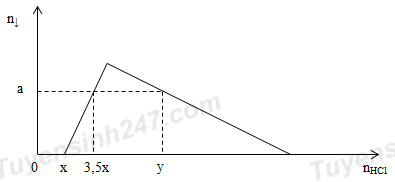
Giá trị của y là
- A 0,18.
- B 0,20.
- C 0,22.
- D 0,81.
Phương pháp giải:
Tính được nH2 = ?
Viết PTHH của Na với nước. Từ nH2 => nNa
=> m Al2O3 = mX – mNa = ? => nAl2O3 = ?
Viết PTHH Al2O3 tác dụng với NaOH => Thành phần dung dịch X gồm: OH- dư (?) và AlO2- (?)
Quan sát đồ thị:
Tại nHCl = x mol: OH- dư vừa bị trung hòa hết => x = nOH- = ?
Tại nHCl = 3,5x = 0,14 mol: nH+ = nOH- + nAl(OH)3 => a = nAl(OH)3 = ?
Tại nHCl = y mol: y = nHCl = nOH- + nAlO2- + 3(nAlO2- - nAl(OH)3) = nOH- + 4nAlO2- - 3nAl(OH)3 = ?
Lời giải chi tiết:
nH2 = 0,08 mol
Gọi số mol Na và Al2O3 lần lượt là x, y (mol)
Na + H2O → NaOH + 0,5H2
0,16 ← 0,16 ← 0,08 (mol)
=> m Al2O3 = mX – mNa = 9,8 – 23.0,16 = 6,12 gam
=> nAl2O3 = 0,06 mol
Al2O3 + 2OH- → 2AlO2- + H2O
0,06 → 0,12dư 0,04→0,12 (mol)
Vậy dung dịch X gồm: OH- dư (0,04 mol) và AlO2- (0,12 mol)
Quan sát đồ thị:
Tại nHCl = x mol: OH- dư vừa bị trung hòa hết => x = nOH- = 0,04 mol
Tại nHCl = 3,5x = 0,14 mol: nH+ = nOH- + nAl(OH)3 => 0,14 = 0,04 + nAl(OH)3
=> a = nAl(OH)3 = 0,1 mol
Tại nHCl = y mol: nHCl = nOH- + nAlO2- + 3(nAlO2- - nAl(OH)3) = nOH- + 4nAlO2- - 3nAl(OH)3
=> y = 0,04 + 4.0,12 – 3.0,1 = 0,22 mol
Đáp án C







