Câu hỏi
Cho 6 g hợp kim Mg và Al vào dung dịch HNO3 đặc, nguội lấy dư thu được 4,48 lít khí NO2 duy nhất bay ra (đktc). Thành phần % về khối lượng của hợp kim là:
- A 20% Mg ; 80% Al
- B 60% Mg ; 40% Al
- C 40% Mg ; 60% Al
- D 80% Mg ; 20% Al
Phương pháp giải:
Phương pháp:
Trong hỗn hợp chỉ có Mg phản ứng với dung dịch HNO3 đặc, nguội.
Bảo toàn e:
ne cho = ne nhận => nMg => mMg
%mMg => %mAl
Lời giải chi tiết:
Hướng dẫn giải:
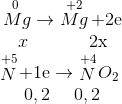
Trong hỗn hợp chỉ có Mg phản ứng với dung dịch HNO3 đặc, nguội .
n= 4,48/22,4 = 0,2 mol => ne nhận = n = 0,2 mol
Bảo toàn e
ne cho = ne nhận => nMg = 0,1 mol => mMg = 24.0,1 = 2,4 g
%mMg = 40%
=> %mAl = 100% - 40% = 60%
Đáp án C.







