Câu hỏi
Hòa tan hoàn toàn hỗn hợp gồm Na2O và 7,14 gam Al2O3 trong nước dư, thu được dung dịch X. Cho từ từ dung dịch HCl 1M đến dư vào X, sự phụ thuộc số mol kết tủa và thể tích dung dịch HCl 1M được biểu diễn theo đồ thị sau:
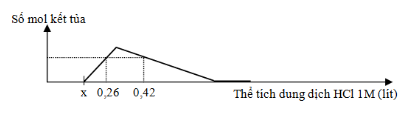
Giá trị của x là
- A 0,14.
- B 0,16
- C 0,12.
- D 0,18.
Phương pháp giải:
Quan sát đồ thị ta thấy phải cho 1 lượng x mol HCl vào mới bắt đầu xuất hiện kết tủa
→ Lượng x mol HCl này dùng để trung hòa NaOH có trong dd X
Vậy dd X chứa: NaAlO2: 0,14 (mol) (BTNT Al) và NaOH: a (mol)
Đặt số mol Al(OH)3 trên đồ thị thu được = b (mol)
Cho từ từ HCl vào dd X xảy ra phản ứng théo thứ tự:
H+ + OH- → H2O (3)
H+ + AlO2‑ + H2O → Al(OH)3↓ (4)
4H+ + AlO2- → Al3+ + 2H2O (5)
Khi nH+= 0,26 thì xảy ra (3) và (4) → nH+ = nOH- + nAl(OH)3 → (I)
Khi nH+ = 0,42 thì xảy ra (3), (4) và (5) → nH+ = nOH- + 4nAlO2‑ - 3nAl(OH)3 → (II)
Giải hệ (I) và (II) ta được a, b = ?
Lời giải chi tiết:
nAl2O3 = 7,14 : 102 = 0,07 (mol)
Na2O + H2O → 2NaOH (1)
2NaOH + Al2O3 → 2NaAlO2 + H2O (2)
Quan sát đồ thị ta thấy phải cho 1 lượng x mol HCl vào mới bắt đầu xuất hiện kết tủa
→ Lượng x mol HCl này dùng để trung hòa NaOH có trong dd X
Vậy dd X chứa: NaAlO2: 0,14 (mol) (BTNT Al) và NaOH: a (mol)
Hay dd X chứa: AlO2-: 0,14 (mol); OH-: a (mol) và Na+
Đặt số mol Al(OH)3 trên đồ thị thu được = b (mol)
Cho từ từ HCl vào dd X xảy ra phản ứng théo thứ tự:
H+ + OH- → H2O (3)
H+ + AlO2‑ + H2O → Al(OH)3↓ (4)
4H+ + AlO2- → Al3+ + 2H2O (5)
Khi nH+= 0,26 thì xảy ra (3) và (4) → nH+ = nOH- + nAl(OH)3 → 0,26 = a + b (I)
Khi nH+ = 0,42 thì xảy ra (3), (4) và (5) → nH+ = nOH- + 4nAlO2‑ - 3nAl(OH)3 → 0,42 = a + 4.0,14 – 3b (II)
Giải hệ (I) và (II) ta được a = 0,16 và b = 0,1
→ x = a = 0,16 (mol)
Đáp án B







