Câu hỏi
Cho 20 gam hỗn hợp gồm Ca và 1 kim loại có tỉ lệ số mol nCa : nM = 3 : 5 tan hết trong dung dịch HCl dư thu được dung dịch A và V lít H2 ở đktc. Cô cạn dung dịch A thu được 48,4 gam chất rắn khan. M là
- A Mg.
- B Al.
- C Ba.
- D Fe.
Phương pháp giải:
Đặt hóa trị của kim loại M là n
Đặt số mol của Ca = 3a (mol); số mol của M là 5a (mol)
PTHH: Ca + 2HCl → CaCl2 + H2O
2M + 2nHCl → 2MCln + nH2↑
BTKL ta có: mCl- = mchất rắn khan – mhh KL = 48,4 – 20 = 28,4 (g)
Sử dụng bảo toàn e
Lời giải chi tiết:
Đặt hóa trị của kim loại M là n
Đặt số mol của Ca = 3a (mol); số mol của M là 5a (mol)
PTHH: Ca + 2HCl → CaCl2 + H2O
2M + 2nHCl → 2MCln + nH2↑
BTKL ta có: mCl- = mchất rắn khan – mhh KL = 48,4 – 20 = 28,4 (g)
=> nCl- = 28,4 : 35,5 = 0,8 (mol)
=> nHCl = nCl- = 0,8 (mol)
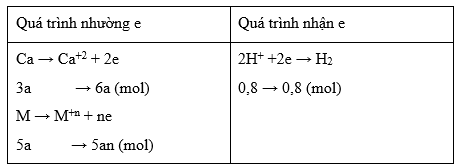
Ta có hệ phương trình:
\(\eqalign{
& \left\{ \matrix{
{m_{hh}} = 40.3a + M.5a = 20\,\,(I) \hfill \cr
\buildrel {BT:e} \over
\longrightarrow 6a + 5an = 0,8\,\,\,\,\,(II) \hfill \cr} \right. \Rightarrow {{(I)} \over {(II)}}co:\,{{120 + 5M} \over {6 + 5n}} = 25 \cr
& \Rightarrow 120 + 5M = 150 + 125n \cr
& \Rightarrow M = 6 + 25n \cr} \)
Vì hóa trị của kim loại thường là 1,2,3 nên chạy thấy n = 2 thì M = 56 (Fe) thỏa mãn
Đáp án D







