Đề bài
Cho kim loại Fe vào dung dịch AgNO3 dư đến khi các phản ứng xảy ra hoàn toàn thì thu được dung dịch X. Các muối trong X là
-
A.
AgNO3 và Fe(NO3)2.
-
B.
Fe(NO3)2, Fe(NO3)3 và AgNO3.
-
C.
Fe(NO3)2 và Fe(NO3)3.
-
D.
Fe(NO3)3 và AgNO3.
Phương pháp giải
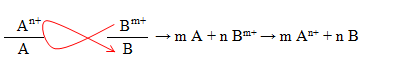
Lời giải của GV Loigiaihay.com
- Ban đầu có phản ứng:
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
- Khi Fe hết, AgNO3 dư thì có phản ứng:
Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
Vậy sau phản ứng thu được các muối: Fe(NO3)3 và AgNO3 dư
Đáp án : D








Danh sách bình luận