Muối Mohr là một muối kép ngậm nước được tạo thành từ hỗn hợp cùng số mol FeSO4.7H2O và (NH4)2SO4 khan:
FeSO4.7H2O + (NH4)2SO4 → FeSO4.(NH4)2SO4.6H2O + H2O
Cho độ tan của muối Mohr ở 20°C là 26,9 gam/100 gam H2O và ở 800C là 73,0 gam/100 gam H2O. Tính khối lượng của muối FeSO4.7H2O cần thiết để tạo thành dung dịch muối Mohr bão hòa 800C, sau khi làm nguội dung dịch này xuống 20°C để thu được 60 gam muối Mohr tinh thể và dung dịch bão hòa. Giả thiết trong quá trình kết tinh nước bay hơi không đáng kể (làm tròn đến hàng phần mười).
Đáp án:
Đáp án:
Dựa vào phương pháp chuẩn độ muối Fe2+
Đặt x là số mol muối Mohr có trong dung dịch bão hòa ở 800C
→ mmuối Mohr = mFeSO4.(NH4)2SO4.6H2O = 392x (g)
ở 800C cứ 73 gam muối Mohr tan được trong 100 gam nước để tạo thành 173 gam dd bão hòa
→ 392x gam muối Mohr.........................?..................................928,9863x gam dd bão hòa
Khi làm nguội dung dịch từ 800C xuống 200C thì tách ra 60 gam muối Mohr tinh thể
→ Khối lượng muối Mohr còn lại trong dung dịch = 392x - 60 (g)
→ Khối lượng dung dịch còn lại = 928,9863x - 60 (g)
Ta có: ở 200C cứ 26,9 gam muối Mohr tan trong 100 gam nước tạo thành 126,9 gam dd bão hòa
Vậy cứ 392x - 60 gam muối Mohr ...........?.............................928,9863x - 60 gam dd bão hòa
→ 26,9 (928,9863x - 60) = 126,9. (392x - 60)
→ x = 0,2424 (mol)
→ mmuối FeSO4.7H2O = 0,2424 × 278 = 68,3871 (gam) 68,4 (gam)

Các bài tập cùng chuyên đề
Xác định số oxi hoá của nguyên tử các nguyên tố chromium và manganese trong các dãy chất sau:
- Cr2O3, CrO3, K2CrO4, K2Cr2O7.
- MnO, MnO2, K2MnO4, KMnO4.
Từ cấu hình electron ở Bảng 27.1, xác định cấu hình electron của các ion kim loại sau: Cr3+, Mn2+, Cu2+.
Thí nghiệm: Xác định hàm lượng muối Fe(ll) bằng dung dịch thuốc tím
- Chuẩn bị:
+ Hoá chất: các dung dịch: KMnO4 0,02 M, H2SO4 10%, FeSO4 có nồng độ khoảng 0,10 M.
+ Dụng cụ: pipette 5 mL, burette 25 mL, bình tam giác 100 mL, ống đong 10 mL, bình tia nước cắt, giá đỡ, kẹp càng cua.
- Tiến hành:
+ Dùng pipette lấy 5,0 mL dung dịch FeSO4 cho vào bình tam giác; thêm tiếp khoảng 5 mL dung dịch H2SO4 10% (lấy bằng ống đong).
+ Cho dung dịch KMnO4 vào burette, điều chỉnh thể tích dung dịch trong burette về mức 0.
+ Mở khoá burette, nhỏ từng giọt dung dịch KMnO4 xuống bình tam giác, lắc đều. Ban đầu dung dịch trong bình tam giác xuất hiện màu hồng rồi mắt màu.
+ Tiếp tục chuẩn độ đến khi màu hồng tồn tại bền trong khoảng 20 giây thì dùng chuẩn độ.
- Ghi lại thể tích dung dịch KMnO4 đã dùng. Tiến hành chuẩn độ 3 lần, ghi số liệu vào vở và xử lí số liệu theo mẫu bảng sau:
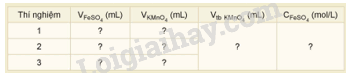
Lưu ý: Trong quá trình chuẩn độ, ban đầu thuốc tim mắt màu chậm, sau đó mắt màu nhanh.
Thí nghiệm: Kiểm tra sự có mặt từng ion riêng biệt: Cu2+, Fe3+.
- Chuẩn bị:
+ Hoá chất: các dung dịch: FeCl3 1 M, CuSO4 1 M, NaOH 1 M.
+ Dụng cụ: ống nghiệm, kẹp ống nghiệm.
- Tiến hành:
+ Cho khoảng 2 mL dung dịch FeCl3 1 M vào ống nghiệm (1) và khoảng 2 mL dung dịch CuSO4 1 M vào ống nghiệm (2).
+ Thêm tiếp vào mỗi ống nghiệm khoảng 2 – 3 giọt dung dịch NaOH 1 M, lắc nhẹ.
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
1. Cho biết màu sắc của các kết tủa tạo thành trong mỗi ống nghiệm.
2. Viết phương trình hoá học của các phản ứng xảy ra trong mỗi ống nghiệm.
Thí nghiệm: Xác định nồng độ của dung dịch FeSO4 bằng dung dịch KMnO4 (dung dịch thuốc tím)
Chuẩn bị:
- Hóa chất: Dung dịch thuốc tím KMnO4 có nồng độ chính xác 0,02M, dung dịch FeSO4 có nồng độ khoảng 0,1M; dung dịch H2SO4 20%
- Dụng cụ: Burette loại 25ml, bình tam giác loại 100ml
Tiến hành:
- Lắp bộ dụng cụ như Hình 20.1. Cho dung dịch thuốc tím vào burette đến vạch 0 đồng thời bảo đảm không còn bọt khí trong burette. Cho 10ml dung dịch FeSO4 và 5ml dung dịch H2SO4 20% vào bình tam giác.
- Mở khóa để nhỏ từ từ từng giọt dung dịch thuốc tím vào bình tam giác, đồng thời lắc đều bình
- Tiếp tục nhỏ dung dịch thuốc tím (vẫn duy trì lắc đều bình) tới khi dung dịch trong bình tam giác xuất hiện màu hồng nhạt bởi một giọt thuốc tím dư, không mất màu trong khoảng 20 giây thì kết thúc chuẩn độ (khóa burette).
- Ghi lại thể tích dung dịch thuốc tím đã dùng. Lặp lại thí nghiệm ít nhất hai lần nữa.
Yêu cầu: Xác định nồng độ của dung dịch FeSO4. Biết phương trình hóa học của phản ứng diễn ra trong quá trình chuẩn độ là:
5Fe2+(aq) + MnO4-(aq) + 8H+(aq) \( \to \)5Fe3+(aq) + Mn2+(aq) + 4H2O(l)
Thí nghiệm 2: Kiểm tra sự có mặt của cation Cu2+ hoặc Fe3+ trong dung dịch
Chuẩn bị:
- Hóa chất: Các dung dịch CuSO4 0,1M; FeCl3 0,1M; NaOH 0,1M.
- Dụng cụ: Ống nghiệm, ống hút nhỏ giọt
Tiến hành:
- Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1ml dung dịch CuSO4
- Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1ml dung dịch FeCl3
Yêu cầu: Quan sát, giải thích hiện tượng và viết phương trình hóa học minh họa.
Một mẫu chất có thành phần chính là muối Mohr. Muối Mohr có công thức hóa học là (NH4)2SO4.FeSO4.6H2O. Hòa tan 0,2151g mẫu chất trong dung dịch sulfuric acid loãng dư, thu được dung dịch có chứa cation Fe2+. Lượng Fe2+ trong dung dịch này phản ứng vừa đủ với 5,40 ml dung dịch thuốc tím nồng độ 0,02M (Các chất và ion khác trong dung dịch không phản ứng với thuốc tím). Xác định
a) Số mg sắt có trong mẫu chất
b) Phần trăm khối lượng của (NH4)2SO4.FeSO4.6H2O trong mẫu chất.
Quan sát Hình 19.1, hãy nhận xét về màu sắc của các ion kim loại chuyển tiếp dãy thứ nhất.
Dự đoán hiện tượng xảy ra trong thí nghiệm xác định hàm lượng muối Fe(ll) bằng dung dịch thuốc tím.
Từ kết quả chuẩn độ, xác định nồng độ Fe2+ trong dung dịch đã pha.
Nêu hiện tượng quan sát được trong thí nghiệm nhận biết các ion Cu2+ và Fe3+, viết phương trình hoá học của phản ứng xảy ra và giải thích.
Để xác định hàm lượng của FeCO3 trong quặng siderite, người ta có thể làm như sau: Cân 0,300 g mẫu quặng, xử lí theo một quỵ trình thích hợp, thu được dung dịch FeSO4 trong môi trường H2SO4 loãng. Coi như dung dịch không chứa tạp chất tác dụng với KMnO4. Chuẩn độ dung dịch thu được bằng dung dịch KMnO4 0,02 M thì dùng hết 12,5 mL. Tính thành phần % theo khối lượng của FeCO3 trong quặng.
Nhỏ vài giọt dung dịch NaOH vào dung dịch FeCl3 thu được kết tủa có màu?
-
A.
keo trắng
-
B.
nâu đỏ
-
C.
xanh lam
-
D.
tím đen
Trong dung dịch muối sulfate, ion kim loại nào sau đây có màu xanh?
-
A.
Mn2+
-
B.
Fe3+
-
C.
Ti3+
-
D.
Cu2+
Hoà \(\tan 0,422\;{\rm{g}}\) mẫu khoáng vật của sắt trong dung dịch sulfuric acid dư, sao cho tất cả lượng sắt có trong quặng đều chuyển thành \({\rm{F}}{{\rm{e}}^{2 + }}\), thu được dung dịch \({\rm{A}}\). Chuẩn độ \({\rm{F}}{{\rm{e}}^{2 + }}\) trong dung dịch \({\rm{A}}\) bằng chất chuẩn là dung dịch thuốc tím \({\rm{KMn}}{{\rm{O}}_4}0,040{\rm{M}}\). Khi đã sử dụng \(23,50\;{\rm{mL}}\) thì phản ứng vừa qua điểm tương đương.
(a) Nếu chỉ có \({\rm{F}}{{\rm{e}}^{2 + }}\) trong dung dịch \({\rm{A}}\) tác dụng được với thuốc tím thì việc chuẩn độ dung dịch \({\rm{A}}\) sẽ giúp xác định được lượng nguyên tố sắt trong mẫu khoáng vật. Từ đó tính được \(\% \) (theo khối lượng) của nguyên tố sắt có trong mẫu khoáng vật là 60,26 %.
(b) Trong quá trình chuẩn độ trên, cần nhỏ từ từ dung dịch thuốc tím từ burette vào bình tam giác chứa dung dịch \({\rm{A}}\).
(c) Cần thêm chất chỉ thị phù hợp vào bình tam giác chứa dung dịch \({\rm{A}}\) để xác định được thời điểm kết thúc quá trình chuẩn độ.
(d) Cần lặp lại thí nghiệm chuẩn độ 2 lần để bảo đảm tính chính xác của kết quả.
Dung dịch FeCl3 có môi trường acid do sự thủy phân của ion Fe3+ theo phản ứng đơn giản hóa:
Fe3+ (aq) + H2O (l) → [Fe(OH)]2+ (aq) + H+(aq) Ka = 10-2,19
Gía trị pH của dung dịch FeCl3 0,1M là
Dựa vào Bảng 20.4 (sách Hoá học 12, bộ sách Cánh Diều), hãy chỉ ra những phát biểu đúng.
(a) Các kim loại chuyển tiếp thường cứng và khó nóng chảy.
(b) Các kim loại chuyển tiếp được xếp vào nhóm kim loại nhẹ.
(c) So với calcium (là kim loại ), các kim loại chuyển tiếp dãy thứ nhất có khối lượng riêng, độ cứng và nhiệt độ nóng chảy thấp hơn.
(d) Nhờ có độ cứng cao, đồng thời bền trước tác động của các tác nhân ăn mòn nên chromium được dùng làm lớp bảo vệ chống ăn mòn cho các dụng cụ, máy móc, thiết bị, đồ gia dụng,...
(e) Do có độ cứng vừa phải và dẫn điện tốt nên đồng được sử dụng làm da dẫn trong các thiết bị và mạng lưới điện gia dụng.
Cho các thông tin sau:
|
Cặp oxi hoá – khử |
Thế điện cực chuẩn (V) |
|
Fe3+/Fe2+ |
-0,77 |
|
Cr2O72- +14H+/2Cr3++7H2O |
1,33 |
|
MnO4- +8H+/Mn2+ + 4H2O |
1,53 |
Biết \({\rm{C}}{{\rm{r}}_2}{\rm{O}}_7^{2 - }(aq)\) có màu cam và \({\rm{C}}{{\rm{r}}^{3 + }}(aq)\) có màu xanh lá cây.
Mỗi phát biểu dưới đây đúng hay sai?
(a) Trong môi trường acid, anion \({\rm{C}}{{\rm{r}}_2}{\rm{O}}_7^{2 - }\) (từ sự phân li của muối potassium dichromate, \({{\rm{K}}_2}{\rm{C}}{{\rm{r}}_2}{{\rm{O}}_7}\) ) có tính oxi hoá mạnh hơn anion \({\rm{MnO}}_4^ - \)(từ sự phân li của muối \({\rm{KMn}}{{\rm{O}}_4}\) ).
(b) Chuẩn độ được \({\rm{F}}{{\rm{e}}^{2 + }}\) trong dung dịch gồm \({\rm{F}}{{\rm{e}}^{2 + }},{\rm{SO}}_4^{2 - }\) và \({{\rm{H}}^ + }\)bằng dung dịch chứa chất chuẩn là \({\rm{KMn}}{{\rm{O}}_4}\).
(c) Không chuẩn độ được \({\rm{F}}{{\rm{e}}^{2 + }}\) trong dung dịch gồm \({\rm{F}}{{\rm{e}}^{2 + }},{\rm{SO}}_4^{2 - }\) và \({{\rm{H}}^ + }\)bằng dung dịch chứa chất chuẩn là \({{\rm{K}}_2}{\rm{C}}{{\rm{r}}_2}{{\rm{O}}_7}\).
(d) Có diễn ra phản ứng oxi hoá - khử theo phương trình hoá học sau:
\(6{\rm{F}}{{\rm{e}}^{3 + }}(aq) + 2{\rm{C}}{{\rm{r}}^{3 + }}(aq) + 7{{\rm{H}}_2}{\rm{O}}(l) \to 6{\rm{F}}{{\rm{e}}^{2 + }}(aq) + {\rm{C}}{{\rm{r}}_2}{\rm{O}}_7^{2 - }(aq) + 14{{\rm{H}}^ + }(aq)\)
Hoà \(\tan 0,422\;{\rm{g}}\) mẫu khoáng vật của sắt trong dung dịch sulfuric acid dư, sao cho tất cả lượng sắt có trong quặng đều chuyển thành \({\rm{F}}{{\rm{e}}^{2 + }}\), thu được dung dịch \({\rm{A}}\). Chuẩn độ \({\rm{F}}{{\rm{e}}^{2 + }}\) trong dung dịch \({\rm{A}}\) bằng chất chuẩn là dung dịch thuốc tím \({\rm{KMn}}{{\rm{O}}_4}0,040{\rm{M}}\). Khi đã sử dụng \(23,50\;{\rm{mL}}\) thì phản ứng vừa qua điểm tương đương.
Mỗi phát biểu dưới đây là đúng hay sai?
(a) Nếu chỉ có \({\rm{F}}{{\rm{e}}^{2 + }}\) trong dung dịch \({\rm{A}}\) tác dụng được với thuốc tím thì việc chuẩn độ dung dịch \({\rm{A}}\) sẽ giúp xác định được lượng nguyên tố sắt trong mẫu khoáng vật. Từ đó tính được \(\% \) (theo khối lượng) của nguyên tố sắt có trong mẫu khoáng vật là 60,26 %.
(b) Trong quá trình chuẩn độ trên, cần nhỏ từ từ dung dịch thuốc tím từ burette vào bình tam giác chứa dung dịch \({\rm{A}}\).
(c) Cần thêm chất chỉ thị phù hợp vào bình tam giác chứa dung dịch \({\rm{A}}\) để xác định được thời điểm kết thúc quá trình chuẩn độ.
(d) Cần lặp lại thí nghiệm chuẩn độ 2 lần để bảo đảm tính chính xác của kết quả.
Giải thích vì sao:
a) có thể phân biệt các dung dịch \({\rm{CuS}}{{\rm{O}}_4},{\rm{CoS}}{{\rm{O}}_4},{\rm{FeS}}{{\rm{O}}_4},{\rm{NiS}}{{\rm{O}}_4}\) và \({\rm{CrS}}{{\rm{O}}_4}\) thông qua quan sát?
b) có thể phân biệt được hai muối \({{\rm{K}}_2}{\rm{Cr}}{{\rm{O}}_4}\) và \({{\rm{K}}_2}{\rm{C}}{{\rm{r}}_2}{{\rm{O}}_7}\) thông qua quan sát?
c) có thể nhận biết cation \({\rm{C}}{{\rm{u}}^{2 + }}\) trong dung dịch bằng dung dịch base?
d) có thể nhận biết cation \({\rm{F}}{{\rm{e}}^{3 + }}\) trong dung dịch bằng dung dịch base?
Tìm hiểu, cho biết những phát biểu nào sau đây là đúng.
(a) Ở dạng đơn chất, sắt là kim loại nặng, có độ hoạt động hoá học mạnh.
(b) Sắt ít được sử dụng ở dạng nguyên chất. Sắt chủ yếu được sử dụng ở dạng hợp kim (thép thường, inox,...).
(c) Đinh đóng gỗ được làm bằng thép nhưng vẫn bị gi sét do ăn mòn điện hoá.
(d) Số oxi hoá của sắt trong các hợp chất FeO, Fe2O3 và FeO.(OH)(H2O)lần lượt là +2 và +3
(e) Thành phần chính của gỉ sét, của váng nâu đỏ ở vùng nước nhiễm phèn là FeO.(OH).H2O hay Fe(OH)3.
Giải thích vì sao:
a) số oxi hoá lớn nhất của nguyên tố manganese là +7 ?
b) hợp chất \({\rm{KMn}}{{\rm{O}}_4}\) có tính oxi hoá mạnh?
c) số oxi hoá lớn nhất của nguyên tố chromium là +6 ?
d) hợp chất \({{\rm{K}}_2}{\rm{Cr}}{{\rm{O}}_4}\) có tính oxi hoá mạnh?
e) sắt là nguyên tố chuyển tiếp?
g) trong tự nhiên, cation \({\rm{F}}{{\rm{e}}^{3 + }}\) thường phổ biến hơn cation \({\rm{F}}{{\rm{e}}^{2 + }}\) ?
h) cation \({\rm{F}}{{\rm{e}}^{2 + }}\) có cả tính oxi hoá và tính khử?
Hợp chất \({\rm{F}}{{\rm{e}}_3}{{\rm{O}}_4}\) được gọi là oxide sắt từ do có từ tính mạnh. Chất này còn có tên gọi là iron(II, III) oxide do đây là hỗn hợp của \({\rm{FeO}}\) và \({\rm{F}}{{\rm{e}}_2}{{\rm{O}}_3}\) theo tỉ lệ mol 1:1.
a) Theo quá trình: \({\rm{F}}{{\rm{e}}_3}{{\rm{O}}_4}(s) + {\rm{HCl}}(aq) \to {\rm{FeC}}{{\rm{l}}_2}(aq) + {\rm{FeC}}{{\rm{l}}_3}(aq) + {{\rm{H}}_2}{\rm{O}}(l)\) thì số mol \({\rm{HCl}}\) trong dung dịch hydrochloric acid cần để hoà tan vừa đủ \(1\;{\rm{molF}}{{\rm{e}}_3}{{\rm{O}}_4}\) là bao nhiêu?
b) Trong tự nhiên, \({\rm{F}}{{\rm{e}}_3}{{\rm{O}}_4}\) là thành phần chính của khoáng vật magnetite, được dùng tạo sắt nóng chảy trong quá trình sản xuất thép.
(b1) Viết phương trình hoá học của phản ứng xảy ra khi khử \({\rm{F}}{{\rm{e}}_3}{{\rm{O}}_4}\) thành sắt bởi carbon monoxide ở nhiệt độ cao.
(b2) Trong phản ứng trên, số electron mà 1 phân tử \({\rm{F}}{{\rm{e}}_3}{{\rm{O}}_4}\) cần nhận để tạo thành sắt là bao nhiêu?
Hãy giải thích tại sao các nguyên tố từ Sc đến Mn đều có khả năng tạo ra các hợp chất với số oxi hoá cao nhất bằng số thứ tự của nhóm nhưng các nguyên tố từ Fe đến Ni lại không có khả năng đó và nguyên tố Cu còn có khả năng tạo ra hợp chất với số oxi hoá +2 phổ biến hơn +1.
Dung dịch X chứa hỗn hợp hai muối FeSO4 và Fe2(SO4)3 trong môi trường H2SO4 loãng. Nếu lấy 10,0 mL dung dịch X, chuẩn độ bằng dung dịch KMnO4 0,02 M thì hết 9,1 mL. Khi lấy 25,00 mL dung dịch X và thêm vào đó lượng dư dung dịch NH3, lọc, rửa kết tủa, nung kết tủa trong không khí đến khối lượng không đổi, cân chất rắn còn lại được 1,2 g.
a. Viết phương trình hoá học của các phản ứng xảy ra.
b. Xác định nồng độ mol của các muối trong dung dịch X. Cho biết các phản ứng xảy ra hoàn toàn.
Trong thí nghiệm xác định hàm lượng muối Fe(ll) bằng dung dịch thuốc tím, nhận xét nào sau đây là không đúng?
A. lon Fe2+ là chất bị oxi hóa. B. H2SO4 là chất tạo môi trường phản ứng.
C. lon \(MnO_4^ - \) là chất bị khử. D. Dung dịch muối Fe(ll) có màu vàng nhạt.
Dung dịch muối chromium(lll) sulfate có lẫn copper(ll) sulfate, sử dụng dung dịch nào sau đây có thể loại bỏ nguyên tố copper ra khỏi muối chromium(lll) sulfate?
A. Dung dịch ammonia. B. Dung dịch xút.
C. Dung dịch barium chloride. D. Dung dịch soda.
Trạng thái oxi hoá phổ biến của Fe và Mn tương ứng là
A. +2, +3 và +2, +4, +7. B. +2, +3 và +2, +4, +6.
C. +2, +3 và +2, +6, +7. D. +2, +6 và +2, +4, +7.
Iron (II)sulfate thường được bảo quản ở dạng muối Mohr màu xanh nhạt có công thức FeSO4.(NH4)2SO4.nH2O
Thực hiện các thí nghiệm sau:
Thí nghiệm 1: Cân 1,96g muối Mohr rồi hòa tan vào nước, sau đó định mức trong bình 50mL. Chuẩn độ 5mL dung dịch vừa pha cần dùng 5mL dung dịch KMnO4 0,02M trong môi trường H2SO4 loãng. Xác định công thức phân tử muối Mohr.
Thí nghiệm 2: Làm lạnh 100g dung dịch muối Mohr bão hòa ở 30oC đến nhiệt độ ổn định ở 0oC thu được m gam muối Mohr kết tinh. Cho độ tan của muối Mohr trong nước ở các nhiệt độ như sau:
|
Nhiệt độ |
0 |
10 |
20 |
30 |
|
Độ tan |
17,2 |
31 |
36,4 |
45 |
Giá trị của m là bao nhiêu?
Các nghiên cứu được thực hiện với một muối carbonate của kim loại M ( hóa trị II)
Nghiên cứu 1: Tiến hành phân tích hàm lượng các nguyên tố, xác định M chiếm 48,2% khối lượng muối
Nghiên cứu 2: Nung nóng muối carbonate tới phản ứng hoàn toàn trong các khí quyển khác nhau:
|
Thí nghiệm |
1 |
2 |
3 |
|
Khí quyển |
N2 |
O2 |
HCl |
Phần trăm chênh lệch giữa khối lượng mẫu chất rắn sau khi nung so với muối ban đầu ở thí nghiệm 2 là a%. Tính a?







Danh sách bình luận