Biểu diễn dạng hình học của ion phức chất tứ diện \({\left[ {{\rm{FeC}}{{\rm{l}}_4}} \right]^ - }\) và ion phức chất bát diện \({\left[ {{\rm{Mn}}{{\left( {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right)}_{\rm{6}}}} \right]^{2 + }}\).
Các phức chất có dạng hình học xác định:
+ Phức chất loại [ML4] thường có dạng hình học tứ diện hoặc vuông phẳng.
+ Phức chất loại [ML6] thường có dạng bát diện.
- Dạng hình học của ion phức chất tứ diện \({\left[ {{\rm{FeC}}{{\rm{l}}_4}} \right]^ - }\):
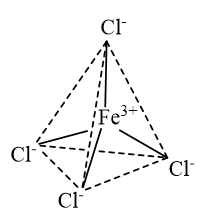
- Dạng hình học của ion phức chất bát diện \({\left[ {{\rm{Mn}}{{\left( {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right)}_{\rm{6}}}} \right]^{2 + }}\):
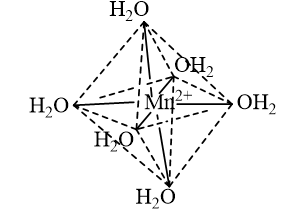

Các bài tập cùng chuyên đề
Phức chất (A) và phức chất (B) có cấu tạo như sau:
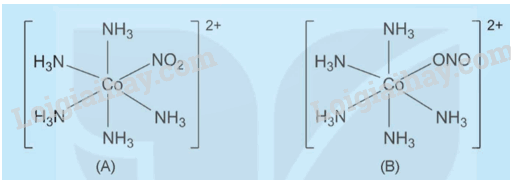
Hãy chỉ ra sự khác nhau về cấu tạo của hai phức chất này.
Cho phức chất: [Ni(NH3)6]2+ và [PdCl2(NH3)4].
a) Phức chất nào có đồng phân cis-, trans-?
b) Vẽ đồng phân cis-, trans- (nếu có) của mỗi phức chất.
Cho các phức chất sau: [Ag(NH3)2]+, [ZnCl4]2-, [Ni(CN)4]2-, [PtCl2(NH3)2] ( vuông phẳng).
a) Phức chất nào có đồng phân cis-, trans-?
b) Vẽ đồng phân cis-, trans- ( nếu có) của mỗi phức chất.
Xét phức chất vuông phẳng có nguyên tử trung tâm M và hai loại phối tử A,B. Cả A và B đều có dung lượng phối trí là 1.
1. Viết các công thức hoá học có thể có của phức chất (bỏ qua điện tích của phức chất).
2. Biểu diễn dạng hình học có thể có của các phức chất.
Biểu diễn dạng hình học của phức chất tứ diện [NiCl4]2- và phức chất bát diện [Fe(H2O)6]3+.
Mô tả sự hình thành phức chất [FeF6]3- theo thuyết liên kết hoá trị. Biết Fe có Z=26.
Dự đoán dạng hình học của phức chất [Ti(H2O)6]3+ và kiểu lai hoá của nguyên tử trung tâm trong phức chất, biết Ti có Z=22.
Biết phức chất [NiCl4]2- có dạng hình học tứ diện.
a) Xác định nguyên tử trung tâm và số phối trí của nguyên tử trung tâm.
b) Trình bày sự hình thành liên kết trong phức chất [NiCl4]2- theo thuyết liên kết hoá trị, biết Ni có Z=28.
Phức chất [CoCl2(en)2]+ có cấu tạo như sau:
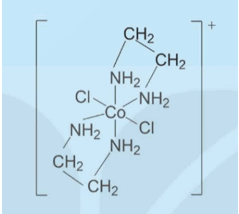
a) Chỉ ra các phối tử trong phức chất trên và dung lượng phối trí của chúng.
b) Chỉ ra nguyên tử trung tâm trong phức chất trên và số phối trí của nó.
c) Nguyên tử trung tâm trong phức chất trên đã nhận cặp electron từ nguyên tử nào của các phối tử?
d) Nêu dạng hình học của phức chất trên.
Xác định nguyên tử trung tâm và kiểu lai hoá của nó trong phức chất [Zn(NH3)4]2+ có dạng hình học tứ diện và phức chất [CoF6]3-.
Trong phức chất [MLn], các phối tử L sắp xếp xung quanh nguyên tử trung tâm M tạo ra các dạng hình học khác nhau. Vậy, sự hình thành liên kết trong phức chất tứ diện và phức chất bát diện được giải thích như thế nào theo thuyết liên kết hoá trị?
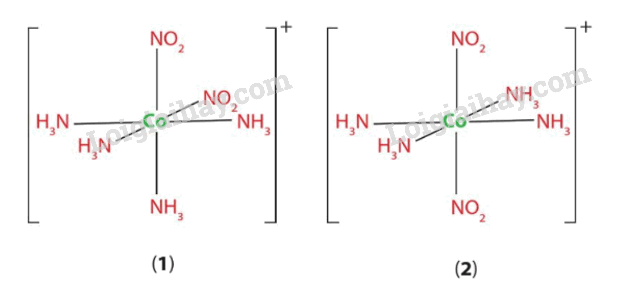
Chỉ ra dạng cis và dạng trans trong hai đồng phân dưới đây:
Phức chất [Co(OH2)6]2+ có dạng hình học bát diện. Giải thích sự tạo thành liên kết và vẽ dạng hình học của phức chất này theo thuyết Liên kết hóa trị.
Phức chất [CoCl4]2- có dạng hình học tứ diện. Giải thích sự tạo thành liên kết và vẽ dạng hình học của phức chất này theo thuyết Liên kết hóa trị.
Hãy cho biết hai phức chất dưới đây có phải là đồng phân của nhau không. Giải thích.
[PtCl2(NH3)4]Br2 và [PtBr2(NH3)4]Cl2.
Vì sao nguyên tử N và một nguyên tử O trong anion \(NO_2^ - \)đều có thể tạo liên kết cho – nhận với nguyên tử trung tâm như trong phức chất (III) hoặc (IV)?
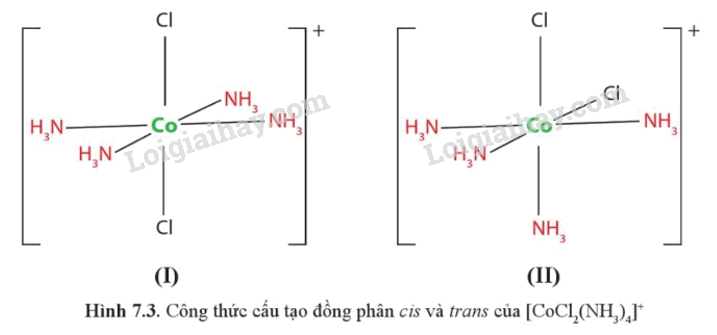
Chỉ ra đồng phân cis và trans của phức chất bát diện [CoCl2(NH3)4]+ ở hình 7.3
Thực nghiệm xác nhận phức chất [Cd(NH3)4]2+ có dạng hình học tứ diện. Hãy vẽ dạng hình học của phức chất này.
Theo thực nghiệm, phức chất [Fe(CN)6]3- có dạng hình học bát diện. Hãy vẽ dạng hình học của phức chất này.
Thực nghiệm xác nhận phức chất [FeF6]4- có dạng hình học bát diện. Giải thích sự hình thành liên kết và mô tả cấu tạo của phức chất này theo thuyết Liên kết hóa trị.
Thực nghiệm xác nhận phức chất [Zn(NH3)4]2+ có dạng hình học tứ diện. Giải thích sự hình thành liên kết và mô tả cấu tạo của phức chất này theo thuyết Liên kết hóa trị.
Xác định điện tích của nguyên tử trung tâm trong phức chất [Cd(NH3)4]2+.
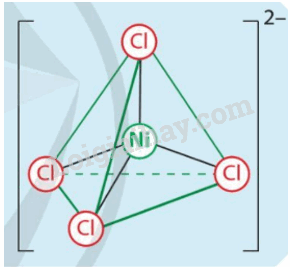
Bằng thực nghiệm, người ta xác định được cấu tạo của phức chất [NiCl4]2- như hình bên. Hãy cho biết:
a) Dạng hình học của phức chất.
b) Thuyết Liên kết hóa trị giải thích dạng hình học của phức chất [NiCl4]2- như thế nào?
Ion phức chất \({\left[ {{\rm{Cr}}{{\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)}_4}{\rm{B}}{{\rm{r}}_{\rm{2}}}} \right]^ + }\) có dạng hình học bát diện. Hãy biểu diễn các đồng phân cis- và trans- của phức chất.
Xác định số phối trí của nguyên tử trung tâm trong các phức chất sau:
a) \({\rm{Na}}\left[ {{\rm{PtC}}{{\rm{l}}_{\rm{5}}}\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)} \right]\);
b) \(\left[ {{\rm{CrC}}{{\rm{l}}_{\rm{3}}}{{\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)}_{\rm{3}}}} \right]\).
Mô tả sự hình thành liên kết, biểu diễn dạng hình học của các ion phức chất sau:
a) Phức chất bát diện \({\left[ {{\rm{Fe}}{{\left( {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right)}_{\rm{6}}}} \right]^{{\rm{3 + }}}}\).
b) Phức chất tứ diện \({\left[ {{\rm{CoB}}{{\rm{r}}_{\rm{4}}}{\rm{ }}} \right]^{{\rm{2 - }}}}\).
Viết công thức đồng phân ion hoá của phức chất \(\left[ {{\rm{CrBr}}{{\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)}_{\rm{5}}}} \right]{\rm{S}}{{\rm{O}}_{\rm{4}}}\).
Biểu diễn các đồng phân cis – trans của phức chất bát diện \(\left[ {{\rm{CrC}}{{\rm{l}}_{\rm{2}}}{{\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)}_{\rm{4}}}} \right]{\rm{Cl}}\)và phức chất vuông phẳng \(\left[ {{\rm{NiC}}{{\rm{l}}_{\rm{2}}}{{\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)}_{\rm{2}}}} \right]\).
Dựa vào Hình 7.6 và 7.7, hãy nêu cách phân biệt đồng phân cis- và đồng phân trans- của phức chất
Hãy dự đoán và biểu diễn dạng hình học của ion phức chất\({\left[ {{\rm{Co}}{{\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)}_6}} \right]^{2 + }}\).







Danh sách bình luận