Khi đun nóng chảy tinh thể NaCl, độ mất trật tự của các ion tăng hay giảm? Tại sao?
Khi đun nóng chảy tinh thể NaCl, độ mất trật tự của các ion tăng vì muối ăn đã chuyển từ trạng thái tinh thể sang trạng thái lỏng.

Các bài tập cùng chuyên đề
Cho phản ứng hóa học: CO2(g) → CO(g) + ½ O2(g) và các dữ kiện:
|
Chất |
O2(g) |
CO2(g) |
CO(g) |
|
\({\Delta _f}H_{298}^o(kJ/mol)\) |
0 |
-393,51 |
-110,05 |
|
\(S_{298}^o(J/mol.K)\) |
205,03 |
214,69 |
-197,50 |
a) Ở điều kiện chuẩn và 25oC phản ứng trên có tự xảy ra được không?
b) Nếu coi \({\Delta _r}{H^o}\) và \({\Delta _r}{S^o}\) không phụ thuộc vào nhiệt độ, hãy cho biết ở nhiệt độ nào phản ứng trên có thể tự xảy ra ở điều kiện chuẩn?
Em hãy dự đoán trong các phản ứng sau, phản ứng nào có ∆S > 0, ∆S < 0 và ∆S ≈ 0. Giải thích.
a) C(s) + CO2(g) → 2CO(g)
b) CO(g) + O2(g) → CO2(g)
c) H2(g) + Cl2(g) → 2HCl(g)
d) S(s) + O2(g) → SO2(g)
e) Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
Quan sát hình dưới: Khi trộn nước và propanol (bên trái) thu được dung dịch (bên phải). Hãy cho biết quá trình đó sẽ làm tăng hay giảm entropy
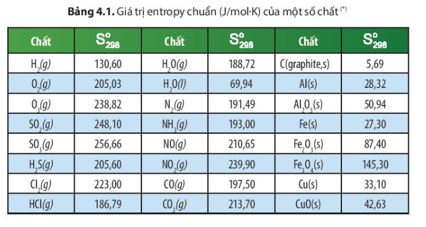
Dựa vào số liệu Bảng 4.1, hãy tính biến thiên entropy chuẩn của các phản ứng sau:
a) SO3(g) → SO2(g) + ½ O2 (g)
và so sánh giá trị \({\Delta _r}S_{298}^o\) của phản ứng này với phản ứng ở ví dụ 1. Giải thích
b) C(graphite, s) + O2 (g)→ CO2(g)
Giải thích tại sao giá trị này lại hơn hơn 0 không đáng kể
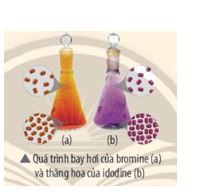
Quan sát bình đựng Br2(l) đang bay hơi (a) và bình đựng I2(s) đang thăng hoa (b) trong hình bên và cho biết các quá trình trên làm tăng hay giảm entropy. Giải thích
Khi chuyển thể của chất từ trạng thái rắn sang lỏng và khí thì entropy của chất tăng hay giảm? Giải thích.
Tại sao khi tăng nhiệt độ lại làm tăng entropy của hệ?
Nếu một lọ nước hoa được mở, chúng ta sẽ ngửi được mùi thơm từ xa, do các phân tử của thành phần nước hoa khuếch tán vào không khí, đó là quá trình tự xảy ra. Ngược lại, để thu hồi các phân tử nước hoa đó vào trong lọ như trạng thái ban đầu thì không thể thực hiện được, đó là quá trình không tự xảy ra. Các phản ứng hóa học cũng tương tự như vậy, có phản ứng tự xảy ra và có phản ứng không tự xảy ra. Các quá trình trong tự nhiên có xu hướng xảy ra theo chiều tăng độ mất trật tự (hỗn loạn) của các tiểu phân trong hệ, người ta gọi đó là quá trình tăng entropy. Entropy là gì? Entropy ảnh hưởng như thế nào đến chiều hướng diễn biến của phản ứng hóa học?
Ở điều kiện thường (coi là 25oC, 1 bar), có tự xảy ra quá trình sắt bị biến đổi thành Fe2O3(s) (có trong thành phần gỉ sắt) được không?
Hãy xác định nhiệt độ thấp nhất để phản ứng nhiệt phân NaHCO3 dưới đây diễn ra:
2NaHCO3(s) → Na2CO3(s) + H2O(l) + CO2(g)
Biết rằng: \({\Delta _r}H_{298}^o\) = 9,16 kJ, \({\Delta _r}S_{298}^o\) được tính theo số liệu cho trong Phụ lục 1. Giả sử biến thiên enthalpy và biến thiên entropy của phản ứng không phụ thuộc vào nhiệt độ.
Hãy đánh giá khả năng tự xảy ra của phản ứng sau ở nhiệt độ chuẩn:
2Al(s) + 3H2O(l) → Al2O3(s) + 3H2(g)
Biết rằng: \({\Delta _r}H_{298}^o\) = -818,3 kJ, \({\Delta _r}H_{298}^o\) được tính theo số liệu cho trong Phụ lục 1. Từ kết quả này hãy đưa ra một số lí do giải thích cho việc vì sao các đồ vật bằng nhôm được sử dụng rất phổ biến.
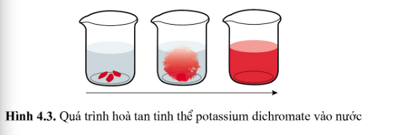
Thả một vài tinh thể patassium dichromate K2Cr2O7 màu cam đỏ vào nước (Hình 4.3). Entropy của quá trình hòa tan này tăng hay giảm? Giải thích.
Tại sao \({\Delta _r}S_{298}^o\) của quá trình (1) lại dương?
Tính \({\Delta _r}S_{298}^o\) của các phản ứng sau:
a) 2Ca(s) + O2(g) → 2CaO(s)
b) CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
c) NH3(g) + HCl(g) → NH4Cl(s)
Tính biến thiên entropy chuẩn cho phản ứng đốt cháy 1 mol CH3OH(l) bằng O2(g), thu được CO2(g) và H2O(g)
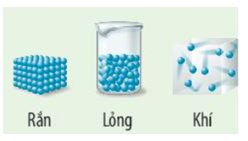
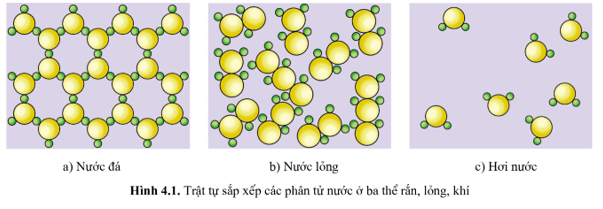
Hình 4.1 mô tả trật tự sắp xếp của các phân tử nước ở ba thể: rắn, lỏng và khí. Em hãy cho biết mức độ “mất trật tự” của hệ tăng hay giảm theo chiều từ nước đá tới hơi nước.
Phản ứng phân hủy của potassium chlorate:
KClO3(s) → KCl(s) + 3/2 O2(g)
Dựa vào các giá trị của \({\Delta _f}H_{298}^0,S_{298}^0\)ở Bảng 4.1 để tính toán và cho biết ở điều kiện chuẩn phản ứng có khả năng tự xảy ra không?
Dựa vào dữ liệu ở Bảng 4.1, tính biến thiên entropy chuẩn của các phản ứng:
a) 4Fe(s) + 3O2(g) → 2Fe2O3(s)
b) SO2(g) + ½ O2(g) → SO3(g)
Biến thiên entropy chuẩn của phản ứng nào dưới đây có giá trị dương?
A. Ag+(aq) + Br-(aq) → AgBr(s)
B. 2C2H6(g) + 3O2(g) → 4CO2(g) + 6H2O(l)
C. N2(g) + 2H2(g) → N2H4(g)
D. 2H2O2(l) → 2H2O(l) + O2(g).
Phản ứng nào dưới đây xảy ra kèm theo sự giảm entropy?
A. N2(g) + O2(g) → 2NO(g).
B. N2O4 (g) → 2NO2(g)
C. 2CO(g) → C(s) + CO2(g)
D. 2HCl(aq) + Fe(s) → FeCl2(aq) + H2(g)
1. Dãy nào dưới đây các chất sắp xếp theo chiều tăng giá trị entropy chuẩn?
A. CO2(s) < CO2(l) < CO2(g).
B. CO2(g) < CO2(l) < CO2(s).
C. CO2(s) < CO2(g) < CO2(l).
D. CO2(g) < CO2(s) < CO2(l).









Danh sách bình luận