Chất được tạo thành từ các cặp nguyên tố sau đây là chất ion hay chất cộng hoá trị?
a) Na và S
b) H và Cl
c) N và H
d) Ca và O
e) K và Cl
Xác định tỉ lệ số nguyên tử của hai nguyên tố trong mỗi hợp chất tạo thành.
* Liên kết ion được hình thành giữa các nguyên tử kim loại và nguyên tử phi kim, nguyên tử kim loại nhường electron, trở thành ion dương, nguyên tử phi kim nhận electron từ kim loại, trở thành ion âm. Các ion trái dấu hút nhau tạo thành liên kết trong hợp chất ion.
- Số electron phi kim nhận thường bằng 8 trừ số vị trí nhóm phi kim.
- Số electron kim loại nhóm A nhường bằng số vị trí nhóm.
* Liên kết cộng hóa trị là liên kết được hình thành bởi sự dùng chung electron giữa hai nguyên tử. Liên kết cộng hóa trị thường là liên kết giữa hai nguyên tử của nguyên tố phi kim với phi kim.
+ Số electron phi kim góp chung sẽ bằng số electron nguyên tử phi kim thiếu để có được 8 electron lớp ngoài cùng. Mỗi cặp electron dùng chung tạo thành một liên kết cộng hóa trị.
a) Na và S
Na là nguyên tố kim loại, S là nguyên tố phi kim nên liên kết tạo thành giữa Na và S là liên kết ion.
Nguyên tử kim loại Na có 1 electron lớp ngoài cùng, để đạt được 8 electron lớp ngoài cùng giống khí hiếm Ne gần nó thì nguyên tử Na nhường 1 electron.
Nguyên tử S có 6 electron lớp ngoài cùng, cần nhận thêm 2 electron để đạt được 8 electron lớp ngoài cùng giống Ar.
→ 2 nguyên tử Na liên kết ion với 1 nguyên tử S.
→ Tỉ lệ: 2Na: 1S
b) H và Cl
H và Cl là nguyên tố phi kim nên liên kết tạo thành giữa H và Cl là liên kết cộng hóa trị.
Mỗi nguyên tử hydrogen có 1 electron, để đạt được lớp electron ngoài cùng bền vững của khí hiếm gần hydrogen là khí helium có 2 electron, nguyên tử hydrogen cần thêm 1 electron và góp chung 1 electron của mình để tạo liên kết cộng hóa trị.
Nguyên tử chlorine có 7 electron lớp ngoài cùng, cần thêm 1 electron để có 8 electron lớp ngoài, nguyên tử chlorine góp chung 1 electron của mình để tạo liên kết cộng hóa trị với một nguyên tử hydrogen.
→ Tỉ lệ: 1H : 1Cl
c) N và H
N và H là nguyên tố phi kim nên liên kết tạo thành giữa N và H là liên kết cộng hóa trị.
Mỗi nguyên tử hydrogen có 1 electron, để đạt được lớp electron ngoài cùng bền vững của khí hiếm gần hydrogen là khí helium có 2 electron, nguyên tử hydrogen cần thêm 1 electron và góp chung 1 electron của mình để tạo liên kết cộng hóa trị.
Nguyên tử nitrogen có 5 electron lớp ngoài cùng, cần thêm 3 electron để có 8 electron lớp ngoài, nguyên tử nitrogen góp chung 3 electron của mình để tạo liên kết cộng hóa trị với ba nguyên tử hydrogen.
→ Tỉ lệ: 1N : 3H
d) Ca và O
Ca là nguyên tố kim loại, O là nguyên tố phi kim nên liên kết tạo thành giữa Ca và O là liên kết ion.
Nguyên tử kim loại Ca có 2 electron lớp ngoài cùng, để đạt được 8 electron lớp ngoài cùng giống khí hiếm Ar gần nó thì nguyên tử Ca nhường 2 electron.
Nguyên tử O có 6 electron lớp ngoài cùng, cần nhận thêm 2 electron để đạt được 8 electron lớp ngoài cùng giống Neon.
→ 1 nguyên tử Ca liên kết ion với 1 nguyên tử O.
→ Tỉ lệ: 1Ca : 1O
e) K và Cl
K là nguyên tố kim loại, Cl là nguyên tố phi kim nên liên kết tạo thành giữa K và Cl là liên kết ion.
Nguyên tử kim loại K có 1 electron lớp ngoài cùng, để đạt được 8 electron lớp ngoài cùng giống khí hiếm Ar gần nó thì nguyên tử K nhường 1 electron.
Nguyên tử Cl có 6 electron lớp ngoài cùng, cần nhận thêm 1 electron để đạt được 8 electron lớp ngoài cùng giống Ar.
→ 1 nguyên tử K liên kết ion với 1 nguyên tử Cl.
→ Tỉ lệ: 1K : 1Cl

Các bài tập cùng chuyên đề
Trong điều kiện thường, nguyên tử của các nguyên tố khí hiếm tồn tại độc lập vì có lớp electron ngoài cùng bền vững. Nguyên tử của các nguyên tố khác luôn có xu hướng tham gia liên kết để có được lớp electron ngoài cùng bền vững tương tự khí hiếm. Vậy liên kết giữa các nguyên tử được hình thành như thế nào?
Quan sát hình 5.1, hãy cho biết số electron ở lớp ngoài cùng của vỏ nguyên tử khí hiếm
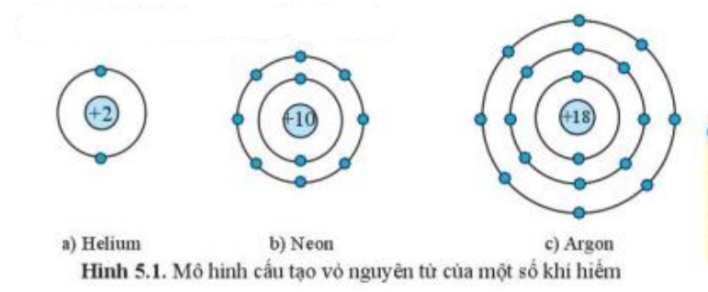
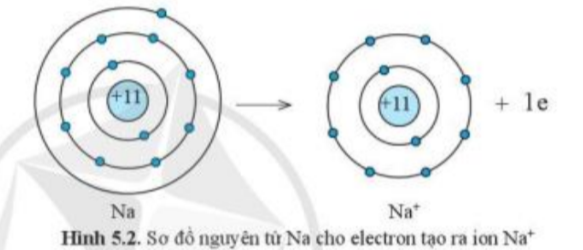
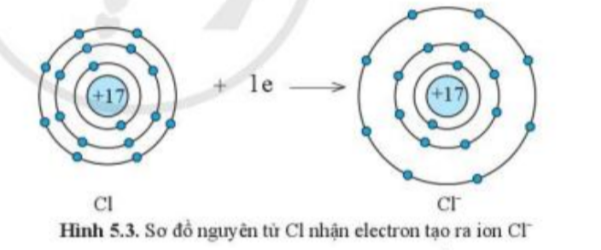
1. Quan sát hình 5.2 và hình 5.3, cho biết lớp vỏ của các ion Na+, Cl- tương tự vỏ nguyên tử của nguyên tố khí hiếm nào.
2. Quan sát hình 5.2, hãy so sánh về số electron, số lớp electron giữa nguyên tử Na và ion Na+
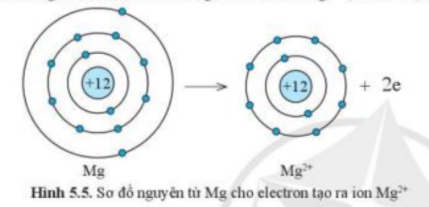
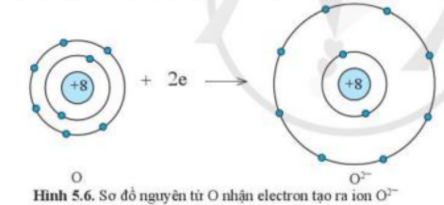
1. Quan sát các hình 5.5 và 5.6, cho biết các ion Mg2+ và O2- có lớp vỏ tương tự khí hiếm nào
2. Quan sát hình 5.5, hãy so sánh về số electron, số lớp electron giữa nguyên tử Mg và ion Mg2+
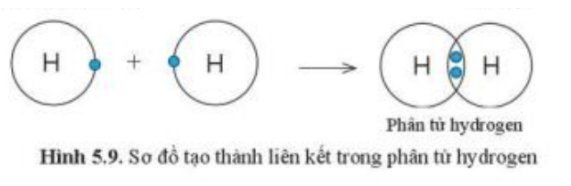
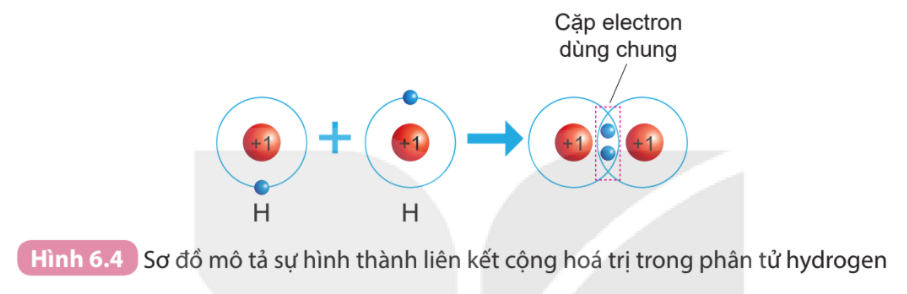
Quan sát hình 5.9, hãy cho biết nguyên tử H trong phân tử hydrogen có lớp vỏ tương tự khí hiếm nào
Hai nguyên tử Cl liên kết với nhau tạo thành phân tử chlorine
a) Mỗi nguyên tử Cl cần thêm bao nhiêu electron vào lớp ngoài cùng để có lớp vỏ tương tự khí hiếm
b) Hãy vẽ sơ đồ tạo thành liên kết trong phân tử chlorine
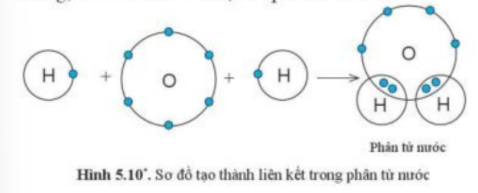
Quan sát hình 5.10, cho biết trong phân tử nước, mỗi nguyên tử H và O có bao nhiêu electron ở lớp ngoài cùng
1. Mỗi nguyên tử H kết hợp với 1 nguyên tử Cl tạo thành phân tử hydrogen chloride. Hãy vẽ sơ đồ tạo thành phân tử hydrogen chloride từ nguyên tử H và nguyên tử Cl
2. Mỗi nguyên tử N kết hợp với 3 nguyên tử H tạo thành phân tử ammonia. Hãy vẽ sơ đồ tạo thành liên kết trong phân tử ammonia.
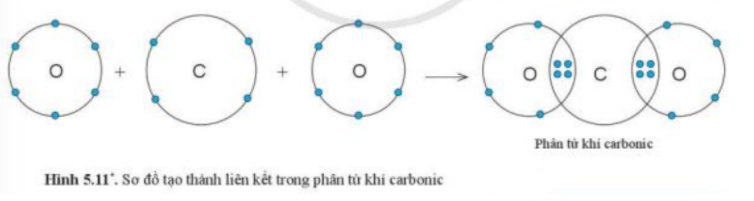
Quan sát hình 5.11, hãy cho biết trong phân tử khí carbonic, nguyên tử C có bao nhiêu electron dùng chung với nguyên tử O
Hãy giải thích các hiện tượng sau:
a) Nước tinh khiết hầu như không dẫn điện, nhưng nước biển lại dẫn được điện.
b) Khi cho đường ăn vào chảo rồi đun nóng sẽ thấy đường ăn nhanh chóng chuyển từ thể rắn sang thể lỏng, làm như vậy với muối ăn thấy muối ăn vẫn ở thể rắn
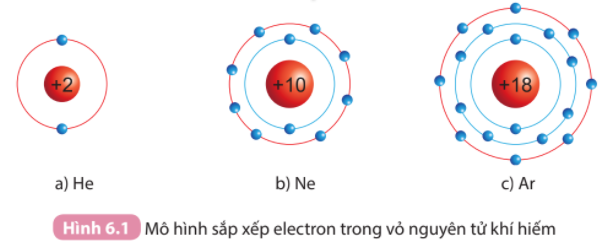
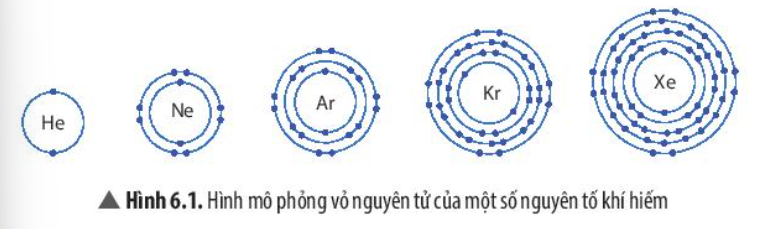
Quan sát Hình 6.1, so sánh số electron lớp ngoài cùng của He, Ne và Ar
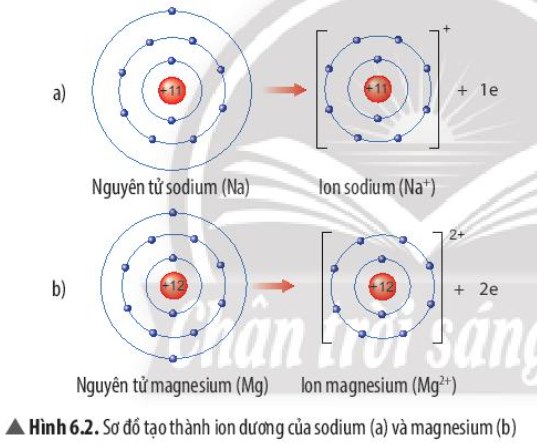
1. Quan sát Hình 6.2 và so sánh số electron ở lớp ngoài cùng của nguyên tử Na, Cl với ion Na+, Cl-.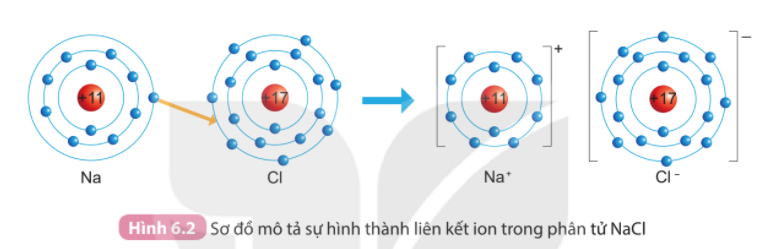
2. Cho sơ đồ mô tả sự hình thành liên kết ion trong phân tử magnesium oxide như sau:

Hãy cho biết nguyên tử Mg đã nhường hay nhận bao nhiêu electron
1. Quan sát Hình 6.4 và Hình 6.5, cho biết số electron lớp ngoài cùng của H và O trước và sau khi tạo thành liên kết cộng hóa trị
2. Hãy mô tả sự hình thành liên kết cộng hóa trị trong phân tử khí chlorine, khí nitrogen
1. Quan sát Hình 6.6 và cho biết khi nguyên tử O liên kết với hai nguyên tử H theo cách dùng chung electron thì lớp vỏ của nguyên tử oxygen giống lớp vỏ của nguyên tử khí hiếm nào?
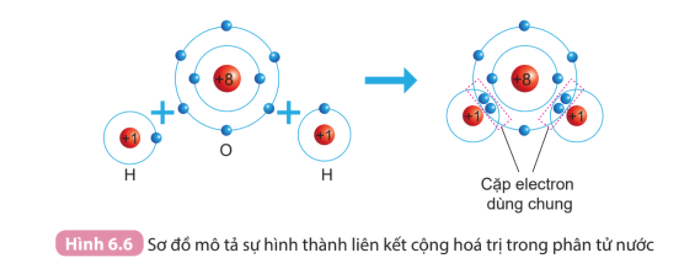
2. Hãy mô tả sự hình thành liên kết cộng hóa trị trong phân tử carbon dioxide, ammonia (gồm một nguyên tử N liên kết với ba nguyên tử H)
Ở điều kiện thường, các nguyên tử khí hiếm thường trơ, bền và chỉ tồn tại độc lập, trong khi các nguyên tử của nguyên tố khác lại có xu hướng kết hợp với nhau.
Các nguyên tử của nguyên tố kết hợp với nhau theo quy tắc nào?
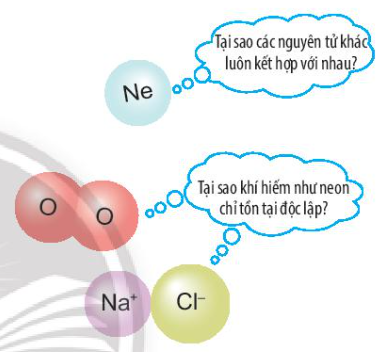
Trừ helium, vỏ nguyên tử của các nguyên tố còn lại ở Hình 6.1 có những điểm giống và khác nhau gì?
Quan sát Hình 6.2, em hãy mô tả sự tạo thành ion sodium, ion magnesium. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
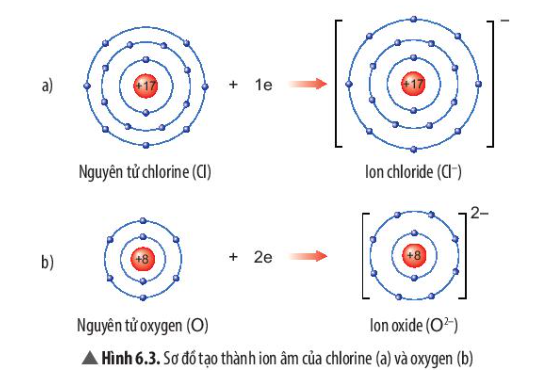
Quan sát Hình 6.3, em hãy mô tả sự tạo thành ion chloride, ion oxide. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
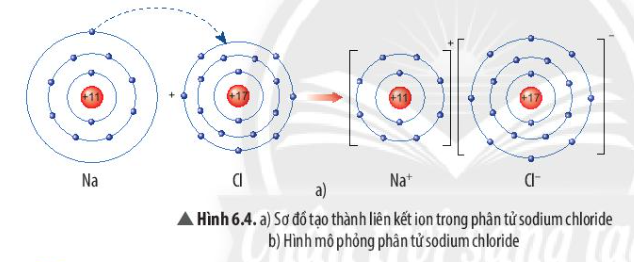
Quan sát Hình 6.4a, em hãy mô tả quá trình tạo thành liên kết ion trong phân tử sodium chloride. Nêu một số ứng dụng của sodium chloride trong đời sống
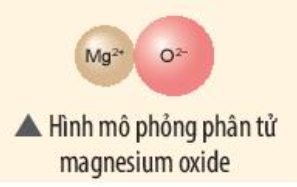
Hãy vẽ sơ đồ và mô tả quá trình tạo thành liên kết ion trong phân tử hợp chất magnesium oxide







Danh sách bình luận