Giải thích vì sao dung dịch HCl dẫn diện tốt hơn dung dịch CH3COOH có cùng nồng độ.
Acid mạnh và base mạnh phân li hoàn toàn trong nước (nên không tồn tại dạng phân tử trong nước). Acid yếu và base yếu phân li một phần trong nước.
HCl là một acid mạnh, trong dung dịch, HCl phân li hoàn toàn: HCl + H2O → H3O+ + Cl-
CH3COOH là một acid yếu, trong dung dịch, CH3COOH phân li không hoàn toàn:
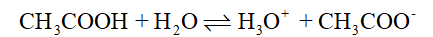
Do đó tuy cùng nồng độ dung dịch HCl dẫn diện tốt hơn dung dịch CH3COOH.

Các bài tập cùng chuyên đề
Cho các dung dịch: HCl, NaOH, Na2CO3.
a) Viết phương trình điện li của các chất trên.
b) Sử dụng máy đo pH (hoặc giấy pH) xác định pH, môi trường (acid/base) của các dung dịch trên.
c) Theo khái niệm acid - base trong môn Hóa học tự nhiên ở lớp 8, trong những chất cho ở trên: Chất nào là acid? Chất nào là base?
Hãy cho biết nguyên nhân vì sao NaCl có tính dẫn điện.
Trong thí nghiệm trên, đèn sáng hay không sáng chứng tỏ tính chất vật lí nào của dung dịch chất tan?
Từ phương trình (1) và (2), nhận xét về mức độ phân li của HCl và CH3COOH trong nước.
Giải thích vai trò của nước trong sự điện li của HCl và NaOH.
Tìm hiểu và cho biết những chất nào sau đây thuộc loại chất điện li: HCl, Fe, BaCl2, Ca(OH)2, CH3COOH, O2.
Kết quả thử tính dẫn điện với các dung dịch hydrochloric acid (HCl), sodium hydroxide (NaOH), saccharose (C12H22O11) ethanol (C2H5OH) được trình bày trong bảng dưới đây. Hãy hoàn thành các thông tin còn thiếu trong bảng vào vở.
Viết phương trình điện li của các chất sau: HF, HI, Ba(OH)2, KNO3, Na2SO4.
Viết phương trình điện li của các chất sau:
- Acid yếu: HCOOH, HCN; acid mạnh: HCl, HNO3.
- Base mạnh: KOH, Ba(OH)2; base yếu: Cu(OH)2.
- Muối: KNO3, Na2CO3, FeCl3.
Hiện nay, năng lượng mà con người sử dụng trong đời sống và sản xuất chủ yếu lấy từ quả trình đốt cháy các nhiên liệu hoá thạch như xăng, dầu, khí đốt tự nhiên và than đá. Một số nhiên liệu hoá thạch, đặc biệt là than đá, có chứa một lượng nhỏ tạp chất sulfur (lưu huỳnh). Trong quá trình đốt cháy, các tạp chất này phản ứng với oxygen tạo thành sulfur dioxide (SO2). Ngoài ra, trong quá trình đốt cháy bất kì nhiên liệu hoá thạch nào, nitrogen từ không khí phản ứng với oxygen tạo thành nitrogen dioxide (NO2). Sulfur dioxide và nitrogen dioxide phản ứng với nước và oxygen (O2) trong khí quyển để tạo thành sulfuric acid và nitric acid:
2SO2 + O2 + 2H2O ⟶ 2H2SO4
4NO2 + O2 + 2H2O ⟶ 4HNO3
Các acid này kết hợp với nước mưa tạo thành mưa acid. Hãy viết phương trình điện li của H2SO4 và HNO3 trong nước, biết rằng H2SO4 điện li theo hai nấc, trong đó nấc thứ nhất điện li hoàn toàn tạo thành và điện li không hoàn toàn ở nấc thứ hai.
“Ợ nóng” là cảm giác đau rát ở thực quản gây ra do sự gia tăng nồng độ hydrochloric acid (HCl) trong dạ dày.
a) Cách đơn giản nhất để giảm chứng ợ nóng nhẹ là nuốt nước bọt nhiều lần do nước bọt có chứa ion bicarbonate (HCO3-), hoạt động như một base, khi nuốt vào sẽ trung hoà một phần acid trong thực quản. Viết phương trình hoá học của phản ứng giữa HCl và HCO3-.
b) Có thể điều trị chứng ợ nóng bằng cách sử dụng các thuốc kháng acid, chẳng hạn “sữa magie” có thành phần chủ yếu là huyền phù Mg(OH)2. Hãy viết phương trình hoá học của phản ứng giữa HCl và Mg(OH)2; giải thích vì sao “sữa magie” hiệu quả hơn nước bọt trong việc trung hoà acid thực quản.
Viết dạng tồn tại chủ yếu trong dung dịch nước của các chất theo bảng sau đây.
|
Chất |
Đặc điểm |
Dạng tồn tại chủ yếu trong dung dịch nước |
|
CH3COOH |
Acid yếu |
|
|
HNO3 |
Acid mạnh |
|
|
C6H12O6 (glucose) |
Chất không điện li |
|
|
NaOH |
Base mạnh |
|
Sodium hydroxide (NaOH) là một chất điện li mạnh, trong khi methanol (CH3OH) là chất không điện li. Hãy mô tả sự khác nhau khi hoà tan các chất trên vào nước. Viết các phương trình minh hoạ.
Viết phương trình điện li trong nước của các chất sau: NaHCO3, CuCl2, (NH4)2SO4, Fe(NO3)3.
Ở cùng nồng độ và cùng điều kiện, chất nào sau đây tạo ra nhiều ion H+ (H3O+) nhất trong dung dịch?
A. Acid mạnh. B. Base mạnh.
C. Acid yếu. D. Nước.
Phương trình mô tả sự điện li của Na2CO3 trong nước là:
\[\begin{array}{l}A.N{a_2}C{O_3}(s) \to 2Na(aq) + C(aq) + 3O(aq)\\B.N{a_2}C{O_3}(s) \to 2N{a^ + }(aq) + {C^{4 + }}(aq) + 3{O^{2 - }}(aq)\\C.N{a_2}C{O_3}(s) \to 2N{a^ + }(aq) + C{O_3}^{2 - }(aq)\\D.N{a_2}C{O_3}(s) \to 2N{a^ + }(s) + C{O_3}^{2 - }(g)\end{array}\]
Phương trình mô tả sự điện li của NaCl trong nước là:
.\[\begin{array}{l}A.NaCl(s) \to Na(aq) + Cl(aq)\\B.NaCl(s) \to N{a^ + }(g) + C{l^ - }(g)\\C.NaCl(s) \to N{a^ + }(aq) + C{l^ - }(aq)\\D.NaCl(s) \to Na(s) + Cl(s)\end{array}\].
Cho các chất: NaOH, HCl, HNO3, NaNO3, saccharose (C12H22O11), ethanol, glycerol, KAl(SO4)2.12H2O. Trong các chất trên, có bao nhiêu chất tạo được dung dịch dẫn điện?
A. 5. B. 3. C. 6. D. 2.
Khả năng dẫn điện của nước vôi trong (dung dịch Ca(OH)2 trong nước) để trong không khí giảm dần theo thời gian. Hãy giải thích điều này.
Tính nồng độ mol của các ion trong các dung dịch sau:
a) Ba(NO3)2 0,1 M.
b) HNO3 0,02 M.
c) КОН 0,01 М.
Viết phương trình điện li của các chất sau trong nước: HBr, HNO3, KOH, Ca(OH)2, Al2(SO4)3, Cu(NO3)2, NaI, HCN, HF, HCOOH.
Cho các chất sau: glucose (C6H12O6), NaCl, KOH, Ba(OH)2, AlCl3, CuSO4, N2, O2, H2SO4, saccharose (C12H22O11). Chất nào là chất điện li trong các chất trên?
Phương trình diện là nào sau đây biểu diễn đúng?
A. \[{\rm{NaOH}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{N}}{{\rm{a}}^{\rm{ + }}}{\rm{ + O}}{{\rm{H}}^ - }\]
B. \[{\rm{HClO}} \to {{\rm{H}}^{\rm{ + }}}{\rm{ + Cl}}{{\rm{O}}^ - }\]
C. \[{\rm{A}}{{\rm{l}}_{\rm{2}}}{{\rm{(S}}{{\rm{O}}_{\rm{4}}}{\rm{)}}_{\rm{3}}} \to 2{\rm{A}}{{\rm{l}}^{{\rm{3 + }}}}{\rm{ + 3SO}}_4^{2 - }\]
D. \[{\rm{N}}{{\rm{H}}_{\rm{4}}}{\rm{Cl}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{NH}}_4^ + {\rm{ + C}}{{\rm{l}}^ - }\]
Phương trình diện là nào sau đây biểu diễn không đúng?
A. \[{\rm{HF}} \to {{\rm{H}}^{\rm{ + }}}{\rm{ + }}{{\rm{F}}^{\rm{ - }}}\]
B.\[{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{CO}}{{\rm{O}}^ - }{\rm{ + }}{{\rm{H}}^{\rm{ + }}}\]
C. \[{\rm{NaCl}} \to {\rm{N}}{{\rm{a}}^{\rm{ + }}}{\rm{ + C}}{{\rm{l}}^ - }\]
D. \[{\rm{NaOH}} \to {\rm{N}}{{\rm{a}}^{\rm{ + }}}{\rm{ + O}}{{\rm{H}}^ - }\]
Các chất trong dãy nào sau đây là những chất điện li mạnh?
A. HCl, NaOH, CH3COOH.
B. KOH, NaCl, H3PO4.
C. HCl, NaOH, NaCl.
D. NaNO3, NaNO2, NH3.
Viết phương trình điện li (nếu có) của các chất trong dung dịch: KBr, NO2, Ca(NO3)2, NaOH, CH4, Ba(OH)2, Fe2(SO4)3, Zn(NO3)2, KI, H2S, CH2=CH-COOH, CuO.
Phương trình điện li nào sau đây không chính xác?
A. \[{\rm{KCl}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {{\rm{K}}^ + } + {\rm{C}}{{\rm{l}}^ - }\].
B. \[{\rm{HCOOH}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{HCO}}{{\rm{O}}^ - } + {{\rm{H}}^ + }\].
C. \[{\rm{HClO}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {{\rm{H}}^ + } + {\rm{Cl}}{{\rm{O}}^ - }\].
D. \[{\rm{Ca(OH}}{{\rm{)}}_{\rm{2}}} \to {\rm{C}}{{\rm{a}}^{2 + }} + {\rm{2O}}{{\rm{H}}^ - }\].
Chất nào sau đây không phải chất điện li?
A. NaCl. B. C6H12O6. C. HNO3. D. NaOH.
Cho các dung dịch sau: HCl 0,1 M; H2SO4 0,1 M và CH3COOH 0,1 M. Sắp xếp các dung dịch trên theo chiều giá trị pH giảm dần. Giải thích.
A. KOH, C2H5OH, H2CO3, MgCl2
B. NaOH, HCl, Ba(NO3)2, H2O
C. NH3, H2S, H2O, HCl
D. HCl, K2SO4, H2SO4, Ca(OH)2







Danh sách bình luận