Thí nghiệm: Kim loại tác dụng với phi kim
- Chuẩn bị:
+ Hoá chất: dây magnesium (Mg), nhôm bột, lưu huỳnh bột.
+ Dụng cụ: kẹp sắt, ống nghiệm chịu nhiệt, đũa thuỷ tinh, đèn cồn.
- Tiến hành:
1. Magnesium tác dụng với oxygen: Dùng kẹp sắt kẹp một mẫu dây magnesium (Mg) và đốt trên ngọn lửa đèn cồn.
2. Nhôm tác dụng với lưu huỳnh: Trộn đều bột nhôm và bột lưu huỳnh theo tỉ lệ khối lượng tương ứng khoảng 1 : 2. Lấy một thìa thuỷ tinh (khoảng 0,3 g) hỗn hợp vào ống nghiệm khô chịu nhiệt. Hơ nóng đều ống nghiệm trên ngọn lửa đèn cồn, sau đó đun tập trung vào phần ống nghiệm chứa hỗn hợp.
Thực hiện yêu cầu sau:
Hãy mô tả hiện tượng quan sát được và viết phương trình hoá học của các phản ứng xảy ra.
Hầu hết các kim loại đều phản ứng với các phi kim điển hình tạo muối học oxide.
1. Magnesium tác dụng với oxygen: Magnesium cháy sáng chói, toả nhiều nhiệt, tạo chất rắn màu trắng.
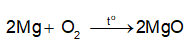
2. Nhôm tác dụng với lưu huỳnh: Hỗn hợp cháy sáng chói, tỏa nhiều nhiệt, tạo thành chất rắn màu trắng.
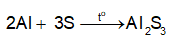

Các bài tập cùng chuyên đề
Khi tác dụng với phi kim, kim loại thể hiện tính chất hoá học gì? Minh hoạ bằng các phương trình hoá học.
Cho các phản ứng sau:
\(\begin{array}{l}{\rm{Fe}} + {\rm{CuS}}{{\rm{O}}_{\rm{4}}} \to {\rm{FeS}}{{\rm{O}}_{\rm{4}}} + {\rm{Cu}}\\{\rm{Cu}} + {\rm{F}}{{\rm{e}}_{\rm{2}}}{{\rm{(S}}{{\rm{O}}_{\rm{4}}}{\rm{)}}_{\rm{3}}} \to 2{\rm{FeS}}{{\rm{O}}_{\rm{4}}} + {\rm{CuS}}{{\rm{O}}_{\rm{4}}}\end{array}\)
Sự sắp xếp các cặp oxi hoá – khử nào sau đây đúng theo thứ tự tăng dần thế điện cực chuẩn?
A. Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+. B. Fe3+/Fe2+; Cu2+/Cu; Fe2+/Fe.
C. Cu2+/Cu; Fe2+/Fe; Fe3+/Fe2+. D. Cu2+/Cu; Fe3+/Fe2+; Fe2+/Fe.
Chuẩn bị:
- Hóa chất: Băng magnesium dài khoảng 3cm – 5 cm.
- Dụng cụ: Đèn cồn, bật lửa, kẹp đốt hóa chất.
Tiến hành: Dùng kẹp đốt hóa chất đưa đoạn băng magnesium vào ngọn lửa đèn cồn.
Yêu cầu: Quan sát và giải thích hiện tượng, viết phương trình hóa học của phản ứng xảy ra.
Viết phương trình hóa học của phản ứng giữa kim loại kẽm với mỗi chất sau: oxygen, sulfur và chlorine.
Dựa vào tính chất vật lí và tính chất hóa học, giải thích vì sao bạc, vàng thường được dùng làm đồ trang sức.
Tiến hành Thí nghiệm 1 và nêu hiện tượng xảy ra. Xác định vai trò của các chất trong các phản ứng hoá học xảy ra ở thí nghiệm này.
Thuỷ ngân dễ bay hơi và rất độc. Khi nhiệt kế thuỷ ngân bị vỡ có thể dùng bột lưu huỳnh để xử lí thuỷ ngân. Giải thích.
Thủy ngân dễ bay hơi và rất độc. Nếu chẳng may nhiệt kế thủy ngân bị vỡ thì dùng chất nào trong các chất sau để khử độc thủy ngân?
-
A.
Bột sắt.
-
B.
Bột lưu huỳnh.
-
C.
Bột than.
-
D.
Nước.
Cho 0,35 mol hỗn hợp X gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
-
A.
75,68%.
-
B.
24,32%.
-
C.
51,35%.
-
D.
48,65%.
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư. (b) Sục khí Cl2 vào dung dịch FeCl2.
(c) Dẫn khí H2 dư qua bột CuO nung nóng. (d) Cho Na vào dung dịch CuSO4 dư.
(e) Nhiệt phân AgNO3. (g) Đốt Fe2S trong không khí.
(h) Điện phân dung dịch CuSO4 với điện cực trơ.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là
-
A.
3
-
B.
4
-
C.
5
-
D.
6
Giải thích vì sao trong tự nhiên hầu như không tìm thấy các oxide của vàng.
Cho một ít bột nhôm vào muỗng đốt hoá chất rồi đốt trên ngọn lửa đèn cồn. Khi một phần bột nhôm trong muỗng cháy đỏ thì đưa nhanh muỗng vào bình chứa oxygen dư. Bột nhôm cháy nhanh và phát ra ánh sáng màu trắng rất mạnh, tạo thành hợp chất \({\bf{A}}\).
Mỗi phát biểu dưới đây đúng hay sai?
(a) Nhôm bị khử tạo thành hợp chất \({\bf{A}}\).
(b) Số oxi hoá của nhôm trong hợp chất \({\bf{A}}\) là +3 .
(c) Biến thiên enthalpy chuẩn của phản ứng giữa nhôm và oxygen có giá trị âm
(\({\Delta _r}H_{298}^o < 0\)).
(d) Phản ứng trên liên quan đến 2 cặp oxi hoá - khử là \({\rm{A}}{{\rm{l}}^{3 + }}/{\rm{Al}}\) và \({{\rm{O}}_2}/2{{\rm{O}}^{2 - }}\).
Dựa vào giá trị thế điện cực chuẩn của các cặp oxi hoá - khử liên quan. hãy cho biết trường hợp nào sau đây không có phản ứng hoá học xảy ra ở điều kiện chuẩn. Viết phương trình hoá học của các phản ứng xảy ra.
a) Cho kẽm (zinc) vào dung dịch tin(II) sulfate.
b) Cho sắt (iron) vào dung dịch magnesium nitrate.
c) Cho chì (lead) vào dung dịch hydrochloric acid.
d) Cho chì vào dung dịch zinc chloride.
e) Cho đồng (copper) vào nước.
Những phát biểu nào sau đây là đúng?
(a) Thông thường, kim loại \({\rm{M}}\) hoạt động càng mạnh thì giá trị thế điện cực chuẩn của cặp oxi hoá - khử \({{\rm{M}}^{\rm{n}}}/{\rm{M}}\) càng âm.
(b) Kim loại \({\rm{M}}\) càng kém hoạt động thì giá trị thế điện cực chuẩn của cặp oxi hoá - khử \({{\rm{M}}^{{\rm{n}} + }}/{\rm{M}}\) càng dương.
(c) Trong cặp oxi hoá - khử \(2{{\rm{H}}_2}{\rm{O}}/\left( {{{\rm{H}}_2} + 2{\rm{O}}{{\rm{H}}^ - }} \right)\)thì \({{\rm{H}}_2}{\rm{O}}\) là dạng khử, \({{\rm{H}}_2}\) là dạng oxi hoá.
(d) Magnesium là kim loại có độ hoạt động hoá học mạnh hơn nhôm (aluminium), giá trị thế điện cực chuẩn của cặp \({\rm{M}}{{\rm{g}}^{2 + }}/{\rm{Mg}}\) âm hơn giá trị thế điện cực chuẩn của cặp \({\rm{A}}{{\rm{l}}^{3 + }}/{\rm{Al}}\).
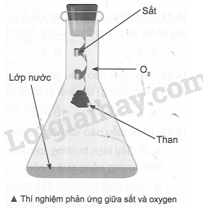
Khi thực hiện thí nghiệm về phản ứng giữa sắt và oxygen, người ta thường cho một ít nước vào trong bình tam giác chứa khí oxygen và cột mẩu than lên thanh dây sắt (như hình bên). Hãy cho biết vai trò của lớp nước dưới đáy bình và mẩu than.
Cho 0,35 mol hỗn hợp X gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%. B. 24,32%. C. 51,35%. D. 48,65%.
Nung nóng hỗn hợp X gồm 3,36 g bột sắt và 1,28 gam bột sulfur ( không có không khí), thu được hỗn hợp Y. Hoà tan Y vào dung dịch HCl dư, thu được hỗn hợp khí Z. Đốt cháy Z cần a mol oxygen. Giá trị của a là bao nhiêu? ( Biết các phản ứng xảy ra hoàn toàn)
Trong trường hợp phải sử dụng kim loại làm đường ống dẫn nước, kim loại nào sau đây là phù hợp nhất để làm ống dẫn nước?
A. Kẽm. B. Sắt. C. Chì. D. Đồng.
Tính chất hoá học đặc trưng của kim loại là
A. tính oxi hoá và tính khử B. tính base C. tính oxi hoá D. tính khử
Cho khí CO (dư) đi qua ống sứ đựng 1,0 g hỗn hợp X gồm Al2O3 và CuO tới khi phản ứng xảy ra hoàn toàn. Dẫn khí đi ra vào nước vôi trong dư, tạo thành 0,4 g kết tủa. Thành phần phần trăm khối lượng CuO trong X là bao nhiêu?
Au, Ag có thể tồn tại được ở dạng đơn chất trong tự nhiên vì chúng là kim loại
A. hoạt động hóa học mạnh. B. hoạt động hóa học trung bình.
C. có khối lượng riêng lớn. D. rất kém hoạt động hóa học.
Những khẳng định nào dưới đây là đúng khi nói về tính chất hóa học của kim loại:
a. Kim loại nhôm tác dụng được với nước. Tuy nhiên phản ứng nhanh chóng dừng lại vì sản phẩm hydroxide không tan ngăn cản nhôm phản ứng với nước
b. Ở nhiệt độ cao magnesium phản ứng với hơi nước để tạo ra hydrogen và magnesium hydroxide
c. Kẽm dễ dàng đẩy đồng ra khỏi dung dịch muối copper (II) sulfate vì kẽm có giá trị thế điện cực chuẩn lớn hơn đồng.
d. Nhôm không phản ứng với nước vì nhôm có giá trị thế điện cực chuẩn EoAl3+/Al = -1,676V thấp hơn thế điện cực của Hydrogen E2H2O/2OH- + H2 = -0,413V.
Một nhà máy luyện kim cần nung chảy một khối đồng (Cu) nặng 64 kg để sản xuất các chi tiết máy. Đồng (Cu) có các thông số sau:
· Nhiệt dung riêng (nhiệt lượng cần để làm tăng nhiệt độ của Cu lên 1 độ) là: 0.385 J/g°C
· Nhiệt nóng chảy (nhiệt lượng cần để làm 1 mol Cu nóng chảy) là: 13.05 kJ/mol
· Nhiệt độ nóng chảy: 1085°C
Tính tổng nhiệt lượng bằng kJ cần thiết để nung chảy khối đồng trên khi nhiệt độ ban đầu là 25oC.
Đốt cháy hết 3,6 g một kim loại hóa trị II trong khí chlorine thu được 14,25 g muối khan của kim loại đó. Kim loại mang đốt là:
Cho 10,8 g kim loại M phản ứng hoàn toàn với khí chlorine dư, thu được 53,4g muối. Phân tử khối của M là?
Nung nóng hỗn hợp X gồm 3,36 g bột sắt và 1,28 gam bột sulfur ( không có không khí), thu được hỗn hợp Y. Hoà tan Y vào dung dịch HCl dư, thu được hỗn hợp khí Z. Đốt cháy Z cần a mol oxygen. Giá trị của a là bao nhiêu? ( Biết các phản ứng xảy ra hoàn toàn)
Một vết nứt trên đường ray tàu hỏa có thể tích 6,72 cm3. Dùng hỗn hợp tecmit (Al và Fe2O3 theo tỉ lệ mol tương ứng 2: 1) để hàn vết nứt trên.
Biết: lượng Fe cần hàn cho vết nứt bằng 79% lượng Fe sinh ra; khối lượng riêng của sắt là 7,9 gam/cm3; chỉ xảy ra phản ứng khử Fe2O3 thành Fe với hiệu suất của phản ứng bằng 96%. Khối lượng của hỗn hợp tecmit tối thiểu cần dùng là? (Làm tròn đến phần nguyên)
Điều nào sau đây là đúng khi nói về tính chất hóa học của kim loại?
-
A.
Tất cả các kim loại đều tác dụng với oxygen tạo thành oxide.
-
B.
Hg tác dụng với sulfur ngay ở nhiệt độ thường nên sulfur được sử dụng để khử độc thủy ngân khi vỡ nhiệt kế thủy ngân trong phòng thí nghiệm.
-
C.
Kim loại Fe tác dụng với phi kim S, Cl2 ra hợp chất sắt (II)
-
D.
Cu có tính khử mạnh hơn Ag nên tác dụng được với dung dịch HCl giải phóng H2.
Một số nước ngầm có chứa nhiều ion Fe2+ (như muối Fe(HCO3)2) ảnh hưởng không tốt khi sử dụng để sinh hoạt, chăn nuôi. Người ta thường sử dụng phương pháp giàn phun mưa để loại bỏ Fe2+ theo phản ứng:
4 Fe(HCO3)2 + O2 + 2H2O → 4Fe(OH)3 + 8CO2.
Có các nhận định sau:
(1) Fe2+ là chất khử.
(2) Xuất hiện kết tủa nâu đỏ.
(3) Có thể tách kết tủa Fe(OH)3 ra khỏi nước bằng phương pháp lọc.
(4) Sử dụng giàn mưa để tăng tốc độ phản ứng oxi hóa ion Fe2+ thành ion Fe3+.
Có bao nhiêu phát biểu đúng?
Có các nhận xét sau:
(a) Cho kim loại silver vào dung dịch iron (II) chloride thì thu được kết tủa silver chloride.
(b) Tất cả các ion kim loại chỉ bị khử.
(c) Ở điều kiện thường, tất cả kim loại đều ở thể rắn, có tính dẻo, dẫn điện, dẫn nhiệt, có ánh kim.
(d) Các kim loại có tính khử mạnh đều khử được copper (II) ion trong dung dịch thành copper.
Số nhận xét không đúng là
-
A.
3
-
B.
1
-
C.
4
-
D.
2







Danh sách bình luận