Cho phản ứng đơn giản: H2 + I2 ⟶ 2HI
Người ta thực hiện ba thí nghiệm với nồng độ các chất đầu (\({C_{{H_2}}}\) và \({C_{{I_2}}}\)) được lấy khác nhau và xác định được tốc độ tạo thành HI trong 20 giây đầu tiên, kết quả cho trong bảng sau:
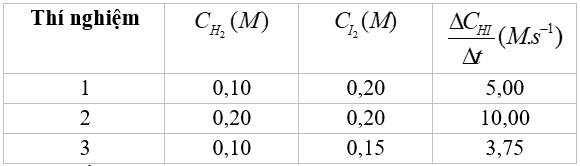
1) Tính tốc độ phản ứng (M.s-1) của các thí nghiệm 1, 2 và 3 ?
2) Viết biểu thức định luật tác dụng khối lượng viết cho phản ứng trên ?
1)
\({\bar v_1} = \frac{1}{2}.\frac{{\Delta {C_{HI}}}}{{\Delta t}} = \frac{1}{2}.5,00 = 2,5M.{s^{ - 1}}\)
\({\bar v_2} = \frac{1}{2}.\frac{{\Delta {C_{HI}}}}{{\Delta t}} = \frac{1}{2}.10,00 = 5M.{s^{ - 1}}\)
\({\bar v_3} = \frac{1}{2}.\frac{{\Delta {C_{HI}}}}{{\Delta t}} = \frac{1}{2}.3,75 = 1,875M.{s^{ - 1}}\)
2) v1 = k.[H2][I2] = 2,5 => k.0,1.0,2 = 2,5 => k = 125
v2 = k.[H2][I2] = 5 => k.0,2.0,2 = 5 => k = 125
v3 = k.[H2][I2] = 1,875 => k.0,1.0,15 = 1,875 => k = 125
biểu thức định luật tác dụng khối lượng trên là: v= 125.[H2][I2]








Danh sách bình luận