Lý thuyết bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Cấu tạo của bảng tuần hoàn các nguyên tố hóa học: chu kì, nhóm, ô nguyên tố
Lý thuyết: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
I. Lịch sử phát minh bảng tuần hoàn các nguyên tố hóa học
- Người ta đã tìm cách phân loại các nguyên tố hóa học khi đã biết một số nguyên tố đáng kể
- Năm 1789, cách phân loại đầu tiên được A. Lavoisier (người Pháp) thực hiện: xếp 33 nguyên tố hóa học thành nhóm các chất khí, kim loại, phi kim và “đất”
- Năm 1829, J.W.Dobereiner (người Đức) phân loại các nguyên tố thành các nhóm có tính chất hóa học giống nhau. Ví dụ: lithium, sodium và potassium là nhóm các kim loại mềm, dễ phản ứng
- Năm 1866, J.Newlands (người Anh) đã xếp các nguyên tố hóa học theo chiều tăng khối lượng nguyên tử thành các octave (quãng tám), trong đó nguyên tử thứ 8 lặp lại tính chất của nguyên tố đầu tiên
- Năm 1869, 2 nhà bác học D.I.Mendeleev (người Nga) và J.L. Meyer (người Đức) đều sắp xếp các nguyên tố theo chiều tăng khối lượng nguyên tử vào các hàng và cột, bắt đầu mỗi hàng (bảng của Mendeleev) hoặc cột mới (bảng của Meyer) khi các tính chất của nguyên tố bắt đầu lặp lại

D.I.Mendeleev
- Trong bảng tuần hoàn các nguyên tố hóa học của Mendeleev, ông đã thay đổi vị trí một số nguyên tố để tính chất của nguyên tố phù hợp với quy luật, đồng thời để trống một số chỗ cho các nguyên tố chưa biết.
- Sau này các nguyên tố ở vị trí còn trống đó được tìm ra và tính chất của chúng đều phù hợp với dự đoán của Mendeleev

- Hiện nay, với những hiểu biết về cấu tạo nguyên tử, bảng tuần hoàn các nguyên tố hóa học hiện đại sắp xếp 118 nguyên tố theo chiều tăng của điện tích hạt nhân nguyên tử
II. Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn
- Bảng tuần hoàn chứa 118 nguyên tố hóa học được sắp xếp theo nguyên tắc sau:
+ Các nguyên tố được sắp xếp theo chiều tăng dần điện tích hạt nhân nguyên tử
+ Các nguyên tố có cùng số electron trong nguyên tử được xếp thành 1 hàng
+ Các nguyên tố có cùng số electron hóa trị trong nguyên tử được xếp thành 1 cột
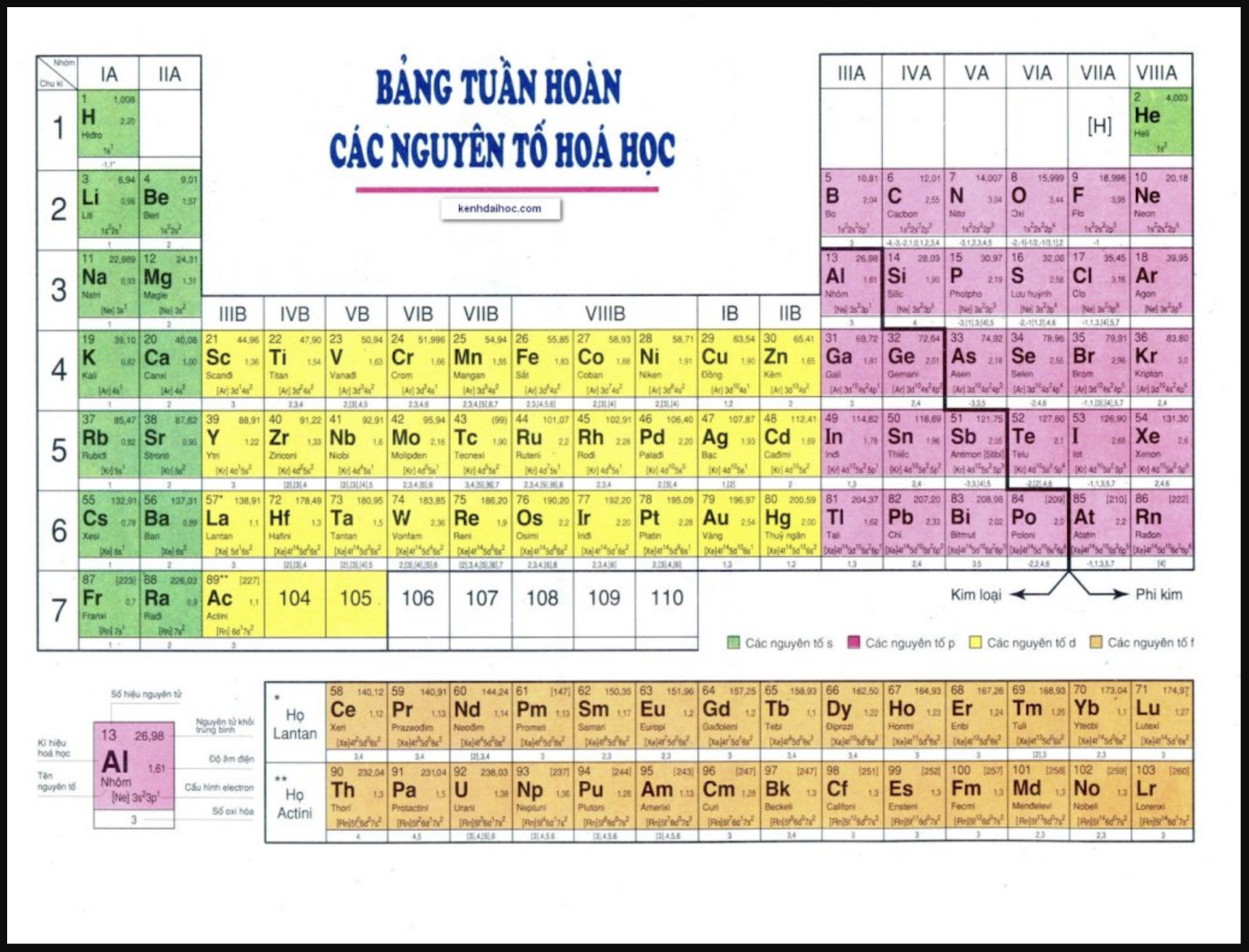
Bảng tuần hoàn các nguyên tố hóa học
- Khi sắp xếp như vậy, sự tuần hoàn tính chất của các đơn chất và hợp chất được thể hiện qua chu kì (hàng) và nhóm (cột)
III. Cấu tạo của bảng tuần hoàn
1. Ô nguyên tố
- Trong bảng tuần hoàn, mỗi nguyên tố được xếp vào một ô, gọi là ô nguyên tố, số thứ tự của ô là số hiệu nguyên tử của nguyên tố đó
- Mỗi ô nguyên tố chứa các thông tin quan trọng nhất về nguyên tố hóa học. Tùy theo từng loại bảng, các thông tin có thể là số hiệu nguyên tử, kí hiệu nguyên tố, tên nguyên tố, nguyên tử khối trung bình
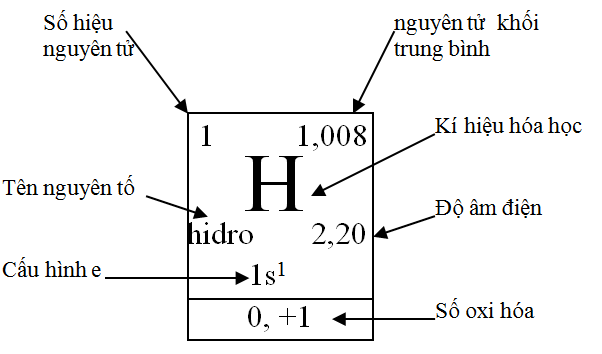
2. Chu kì
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp theo chiều điện tích hạt nhân tăng dần.
- Bảng tuần hoàn hiện nay có 7 chu kì. Số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố trong chu kì.
+ Chu kì 1: gồm 2 nguyên tố H và He, đều có 1 lớp electron.
+ Chu kì 2: gồm 8 nguyên tố từ Li đến Ne, đều có 2 lớp electron.
+ Chu kì 3: gồm 8 nguyên tố từ Na đến Ar, đều có 3 lớp electron.
+ Chu kì 4: gồm 18 nguyên tố từ K đến Kr, đều có 2 lớp electron.
+ Chu kì 5: gồm 18 nguyên tố từ Rb đến Xe, đều có 5 lớp electron.
+ Chu kì 6(*): gồm 32 nguyên tố từ Cs đến Rn, đều có 6 lớp electron.
+ Chu kì 7(*): gồm 32 nguyên tố từ Fr đến Og, đều có 7 lớp electron.
3. Nhóm nguyên tố
- Nhóm nguyên tố gồm các nguyên tố mà nguyên tử của chúng có cấu hình electron tương tự nhau, do đó có tính chất hóa học gần giống nhau và được xếp thành một cột.
- Bảng tuần hoàn hiện nay có 18 cột, chia thành 8 nhóm A (IA đến VIIIA) và 8 nhóm B (IB đến VIIIB). Mỗi nhóm là một cột, riêng nhóm VIIIB gồm 3 cột.
Ví dụ: Nhóm IA -nhóm các kim loại kiềm, nhóm VIIA - nhóm các halogen.
- Nguyên tử các nguyên tố trong cùng 1 nhóm A có số electron hóa trị bằng nhau và bằng số thứ tự của nhóm (trừ He).
4. Phân loại nguyên tố
a. Theo cấu hình electron
- Các nguyên tố s, p, d, f là những nguyên tố mà nguyên tử có electron cuối cùng được điền vào phân lớp s, p, d, f tương ứng
Ví dụ:
11Na: 1s22s22p63s1 (nguyên tố s)
13Al: 1s22s22p63s23p1 (nguyên tố p)
- Các nhóm A: gồm các nguyên tố nhóm s (IA, IIA) và các nguyên tố p (từ IIA đến VIIIA trừ He)
- Các nhóm B: gồm các nguyên tố d (từ IB đến VIIIB) và các nguyên tố f (lanthanides và actinides)

b. Theo tính chất hóa học
- Các nhóm IA, IIA, IIIA: gồm các nguyên tố s và p là kim loại (trừ H và B)
- Các nhóm VA, VIA, VIIA: gồm các nguyên tố p, thường là phi kim
- Nhóm VIIIA: gồm các nguyên tố khí hiếm
- Các nhóm B: gồm các nguyên tố d và f đều là kim loại chuyển tiếp
Luyện Bài Tập Trắc nghiệm Hóa 10 - Kết nối tri thức - Xem ngay












Danh sách bình luận