Bài 17. Phenol trang 53, 54, 55 SBT Hoá 11 Cánh diều
Chất nào sau đây là chất rắn ở điều kiện thường?
Tổng hợp đề thi học kì 2 lớp 11 tất cả các môn - Cánh diều
Toán - Văn - Anh - Lí - Hóa - Sinh
17.1
Chất nào sau đây là chất rắn ở điều kiện thường?
A. Phenol. B. Ethanol. C. Toluene. D. Glycerol.
Phương pháp giải:
dựa theo tính chất vật lý của phenol.
Lời giải chi tiết:
Đáp án A.
17.2
Phenol không phản ứng với chất nào sau đây?
A. NaHCO3 B. Na C. NaOH D. Br2
Phương pháp giải:
Dựa theo tính chất hóa học của phenol.
Lời giải chi tiết:
Đáp án A.
17.3
Trong các chất sau, chất nào thuộc loại phenol?
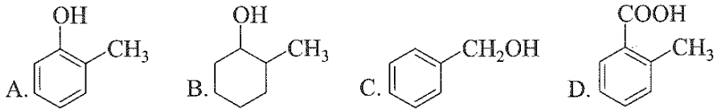
Phương pháp giải:
Phenol là những hợp chất hữu cơ trong phân tử có một hay nhiều nhóm hydroxyl liên kết trực tiếp với nguyên tử carbon của vòng benzene.
Lời giải chi tiết:
Đáp án A.
17.4
Chất nào sau đây tác dụng với theo tỉ lệ mol 1:1 ?
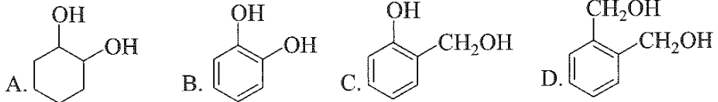
Phương pháp giải:
Các nhóm OH liên kết trực tiếp với vòng benzene sẽ phản ứng với NaOH.
Lời giải chi tiết:
Đáp án C.
17.5
Khi bị bỏng do tiếp xúc với phenol, cách sơ cứu đúng là rửa vết thương bằng dung dịch nào sau đây?
A. Giấm (dung dịch có acetic acid).
B. Dung dịch NaCl
C. Nước chanh (dung dịch có citric acid).
D. Xà phòng có tính kiềm nhẹ.
Phương pháp giải:
dựa theo tính chất hóa học của phenol.
Lời giải chi tiết:
Đáp án D.
17.6
Catechin là một chất kháng oxi hoá mạnh, ức chế hoạt động của các gốc tự do nên có khả năng phòng chống bệnh ung thư, nhồi máu cơ tim. Trong lá chè tươi, catechin chiếm khoảng 25-35% tổng trọng lượng khô. Ngoài ra, catechin còn có trong táo, lê, nho,... Công thức cấu tạo của catechin cho như hình bên:
Phát biểu nào sau đây là không đúng?
A. Công thức phân tử của catechin là C15H14O6
B. Phân tử catechin có 5 nhóm phenol.
C. Catechin phản ứng được với dung dịch NaOH
D. Catechin thuộc loại hợp chất thơm.
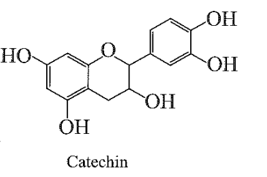
Phương pháp giải:
Phenol là những hợp chất hữu cơ trong phân tử có một hay nhiều nhóm hydroxyl liên kết trực tiếp với nguyên tử carbon của vòng benzene.
Lời giải chi tiết:
Đáp án B.
17.7
Cho gam hỗn hợp gồm phenol và ethanol phản.ứng hoàn toàn với Na dư, thu được 1239,5 ml khí H2 (đo ở điều kiện chuẩn 25C, 1 bar). Mặt khác, gam phản ứng tối đa với 100ml dung dịch NaOH 0,5M. Giá trị của m là
A. 10,5 .
B. 7,0 .
C. 14,0 .
D. 21,0 .
Cho gam hỗn hợp gồm phenol và ethanol phản.ứng hoàn toàn với Na dư, thu được 1239,5 ml khí H2 (đo ở điều kiện chuẩn 25C, 1 bar). Mặt khác, gam phản ứng tối đa với 100ml dung dịch NaOH 0,5M. Giá trị của m là
A. 10,5 .
B. 7,0 .
C. 14,0 .
D. 21,0 .
Phương pháp giải:
Dựa theo tính chất hóa học của phenol và ethanol viết PTPU.
Lời giải chi tiết:
Số mol H2: \(\frac{{1239,5}}{{1000.24,79}} = 0,05(mol)\)
Số mol NaOH: \(\frac{{100}}{{1000}} = 0,05mol\)
Chỉ có phenol tác dụng với NaOH
PTHH:
\({C_6}{H_5}OH + NaOH \to {C_6}{H_5}ONa + {H_2}O\)
0,05 0,05
\({C_6}{H_5}OH + Na \to {C_6}{H_5}ONa + \frac{1}{2}{H_2}\)
0,05 0,025
\({C_2}{H_5}OH + Na \to {C_2}{H_5}ONa + \frac{1}{2}{H_2}\)
0,05 0,025
Khối lượng của hỗn hợp X là: m = 0,05.94 + 0,05.46 = 7,0 (gam).
17.8
Picric acid có nhiều ứng dụng trong y học (định lượng creatinine để chẩn đoán và theo dõi tình trạng suy thận; khử trùng và làm khô da khi điều trị bỏng,...), trong quân sự (sản xuất đạn, thuốc nổ,...), trong phòng thí nghiệm (nhuộm mẫu, làm thuốc thử,...).
a) Viết phương trình hoá học của phản ứng điều chế picric acid từ phenol.
b) Giải thích vì sao trong phòng thí nghiệm thường bảo quản picric acid trong lọ dưới một lớp nước và trong quá trình làm việc với picric acid, tránh để acid tiếp xúc với kim loại?
Phương pháp giải:
Dựa theo tính chất hóa học của phenol.
Lời giải chi tiết:
a) 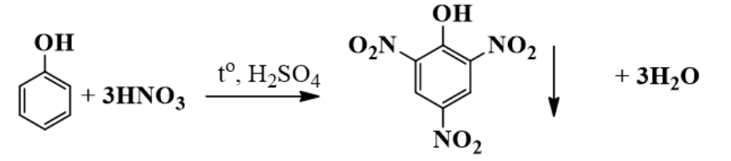
b) Phân tử picric acid dễ gây cháy, nổ mạnh nên để an toàn, thường bảo quản picric acid trong lọ dưới một lớp nước. Mặt khác, picric acid có tính acid mạnh, phản ứng với kim loại toả nhiệt, tạo muối picrate cũng dễ gây cháy nổ.
17.9
Phân tử chất A có một nguyên tử oxygen và một vòng benzene. Trong A phần trăm khối lượng các nguyên tố C, H và O lần lượt là: 77,78%; 7,41% và 14,81%
a) Tìm công thức phân tử của A
b) Cho một lượng chất A vào ống nghiệm đựng nước, thấy A không tan. Thêm tiếp dung dịch NaOH vào ống nghiệm, khuấy nhẹ, thấy A tan dần. Tìm công thức cấu tạo có thể có của A
c) Chất B (phân tử có vòng benzene) là một trong số các đồng phân của A Chất không tác dụng với , không tác dụng với NaOH. Tìm công thức cấu tạo và gọi tên A
Phương pháp giải:
từ % các nguyên tố tìm ra được công thức thực nghiệm. Sau đó tìm ra công thức phân tử và công thức cấu tạo.
Lời giải chi tiết:
a) Gọi công thức của A là CxHyOz
\(x:y:z = \frac{{\% C}}{{12}}:\frac{{\% H}}{1}:\frac{{\% O}}{{16}} = \frac{{77,78\% }}{{12}}:\frac{{7,41}}{1}:\frac{{14,81}}{{16}} = 7:8:1\)
Công thức thực nghiệm của A là (C7H8O)n.
Do A chứa 1 nguyên tử O nên công thức phân tử của A là C7H8O.
b) Thí nghiệm chứng tỏ A không tan trong nước, A tác dụng với NaOH, vậy A là phenol. Công thức cấu tạo của A là một trong số ba công thức cấu tạo sau:
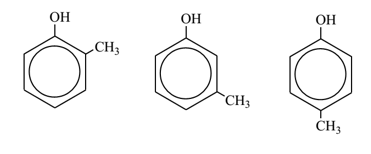
c) Chất B là một trong số các đồng phân (có vòng benzene) của A. Chất B không tác dụng với Na, không tác dụng với NaOH nên B là methyl phenyl ether:
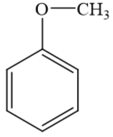
17.10
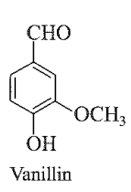
Đề bài: Trong vỏ quả cây vanilla có hợp chất mùi thơm dễ chịu, tên thường là vanillin. Công thức cấu tạo của vanillin là:
a) Viết công thức phân tử của vanillin.
b) Dự đoán khả năng tan trong nước, trong ethanol và trong dung dịch kiềm như NaOH, KOH của vanillin.
c) Mẫu vanillin đủ tiêu chuẩn dùng trong công nghiệp sản xuất dược phẩm và thực phẩm cần có trên 99% về khối lượng là vanillin. Để định lượng một mẫu vanillin, người ta làm như sau: Hoà tan 0,120 gam mẫu trong 20ml ethanol 96% và thêm 60ml nước cất, thu được dung dịch X . Biết X phản ứng vừa đủ với 7,82ml dung dịch nồng độ 0,1M và tạp chất trong mẫu không phản ứng với NaOH . Mẫu vanillin trên có đủ tiêu chuẩn dùng trong công nghiệp sản xuất dược phẩm và thực phẩm không?
Phương pháp giải:
Từ công thức cấu tạo đưa ra công thức phân tử và tính chất của hợp chất.
Lời giải chi tiết:
a) Công thức phân tử của vanillin: C8H8O3
b) Vanillin khó tan trong nước, dễ tan trong ethanol, tan trong dung dịch kiềm do có nhóm OH phenol.
c) Số mol NaOH là: \(\frac{{7,82.0,1}}{{1000}}.108 = {7,82.10^{ - 4}}\) mol
HO – C6H3(OCH3)(CHO) + NaOH => NaO – C6H3(OCH3)(CHO) + H2O
n C8H8O3 = n NaOH = 7,82 . 10-4
Phần trăm khối lượng vanillin trong mẫu trên là:
\(\frac{{{{7,82.10}^{ - 4}}.152}}{{0,12}}.100\% = 99,05\% \)
Vậy mẫu vanillin trên đủ tiêu chuẩn dùng trong công nghiệp sản xuất dược phẩm và thực phẩm.
17.11
Cho biết ở điều kiện nhiệt độ và áp suất cao, xảy ra phản ứng thế nguyên tử halogen (liên kết trực tiếp với vòng benzene) bằng nhóm -OH
a) Viết phương trình hoá học của phản ứng xảy ra khi đun nóng hỗn hợp chlorobenzene và dung dịch đặc, dư ở nhiệt độ 300C áp suất 200 bar.
b) Lập sơ đồ điều chế phenol từ benzene và các chất vô cơ.
c) Tính khối lượng benzene cần thiết để điều chế được 9,4kg phenol theo sơ đồ ở phần b), biết hiệu suất của cả quá trình là 42% .
Phương pháp giải:
Dựa theo tính chất hóa học của phenol.
Lời giải chi tiết:
b) Sơ đồ điều chế phenol từ hợp chất vô cơ: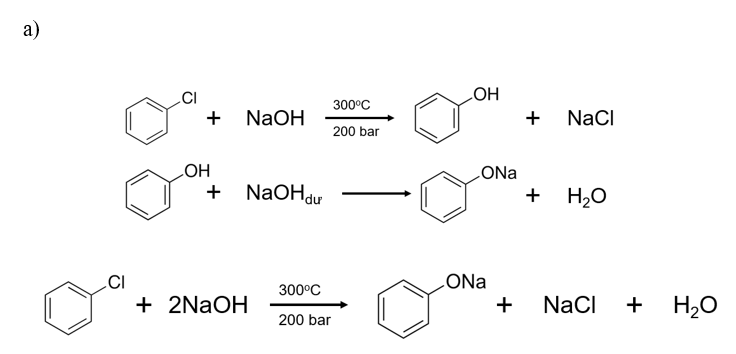
b) Sơ đồ điều chế phenol từ hợp chất vô cơ:
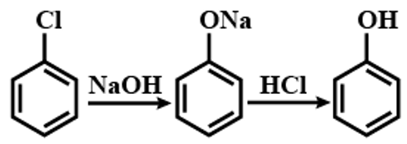
c) \(\begin{array}{l}{n_{phenol}} = {n_{benzen}} = \frac{{9,4}}{{94}} = 0,1\\{m_{benzen}} = \frac{{0,1.78.100}}{{48}} = 18,7kg\end{array}\)
Các bài khác cùng chuyên mục
- Bài 19. Caboxylic acid trang 60, 61, 62, 63, 64 SBT Hoá 11 Cánh diều
- Bài 18. Hợp cất carbonyl trang 56, 57, 58, 59, 60 SBT Hoá 11 Cánh diều
- Bài 17. Phenol trang 53, 54, 55 SBT Hoá 11 Cánh diều
- Bài 16. Alcohol trang 50, 51, 52, 53 SBT Hoá 11 Cánh diều
- Bài 15. Dẫn xuất halogen trang 48, 49, 50 SBT Hóa 11 Cánh diều
- Bài 19. Caboxylic acid trang 60, 61, 62, 63, 64 SBT Hoá 11 Cánh diều
- Bài 18. Hợp cất carbonyl trang 56, 57, 58, 59, 60 SBT Hoá 11 Cánh diều
- Bài 17. Phenol trang 53, 54, 55 SBT Hoá 11 Cánh diều
- Bài 16. Alcohol trang 50, 51, 52, 53 SBT Hoá 11 Cánh diều
- Bài 15. Dẫn xuất halogen trang 48, 49, 50 SBT Hóa 11 Cánh diều




















