Bài 20. Sơ lược về phức chất và sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch trang 115, 116, 117 Hóa 12 Chân trời sáng tạo
Trong dung dịch, hầu hết các ion kim loại chuyển tiếp đều có màu.
CH tr 115 MĐ
Trả lời câu hỏi Mở đầu trang 115 SGK Hóa 12 Chân trời sáng tạo
Trong dung dịch, hầu hết các ion kim loại chuyển tiếp đều có màu. Các ion kim loại chuyển tiếp tồn tại trong nước dưới dạng phức chất aqua. Phức chất gồm những thành phần gì? Trong phức chất tồn tại loại liên kết nào? Phức chất có những tính chất và ứng dụng gì?
Phương pháp giải:
Nêu thành phần, loại liên kết, tính chất và ứng dụng của phức chất.
Lời giải chi tiết:
- Trong thành phần của phức chất có nguyên tử trung tâm và phối tử.
- Liên kết giữa phối tử và nguyên tử trung tâm là liên kết cho – nhận.
- Tính chất của phức chất: phản ứng thế phối tử của phức chất trong dung dịch.
- Ứng dụng: Phức chất có nhiều ứng dụng trong các lĩnh vực khác nhau như y học, dược học, hoá học,...
CH tr 116 TL1
Trả lời câu hỏi Thảo luận 1 trang 116 SGK Hóa 12 Chân trời sáng tạo
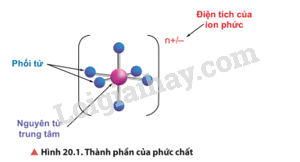
Hãy cho biết thành phần của phức chất được thể hiện trong Hình 20.1.
Phương pháp giải:
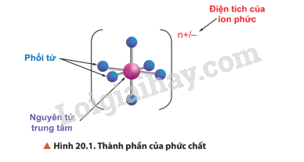
Lời giải chi tiết:
Thành phần của phức chất có nguyên tử trung tâm và phối tử.
CH tr 116 TL2
Trả lời câu hỏi Thảo luận 2 trang 116 SGK Hóa 12 Chân trời sáng tạo
Quan sát Hình 20.2, cho biết dạng hình học của mỗi ion phức chất.
Phương pháp giải:
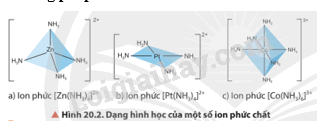
Lời giải chi tiết:
Các dạng hình học của phức chất là tứ diện, vuông phẳng và bát diện.
CH tr 116 LT
Trả lời câu hỏi Luyện tập trang 116 SGK Hóa 12 Chân trời sáng tạo
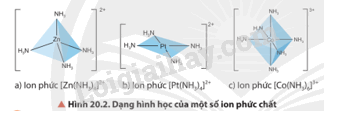
Hãy cho biết nguyên tử trung tâm và phối tử trong các ion phức ở Hình 20.2.
Phương pháp giải:
Lời giải chi tiết:
|
|
Nguyên tử trung tâm |
Phối tử |
|
Hình 20.2a |
Zn2+ |
NH3 |
|
Hình 20.2b |
Pt2+ |
NH3 |
|
Hình 20.2c |
Co3+ |
NH3 |
CH tr 117 TL1
Trả lời câu hỏi Thảo luận 1 trang 117 SGK Hóa 12 Chân trời sáng tạo
Quan sát Hình 20.3, hãy cho biết màu sắc của dung dịch CuSO4. Màu sắc đó là của phức chất aqua nào?
Phương pháp giải:
Chất điện li khi tan vào nước sẽ phân li thành các ion. Các ion không tồn tại độc lập, chúng ở dạng các tiểu phân được bao quanh bởi các phân tử nước. Trong dung dịch, cation kim loại tồn tại dưới dạng phức chất aqua, các phân tử nước là phối tử.
Hầu hết phức chất aqua của ion kim loại chuyển tiếp dãy thứ nhất đều có màu. chúng thường có dạng [M(H2O)6]n+.
Lời giải chi tiết:
Dung dịch CuSO4 có màu xanh lam. Đây là màu sắc của [Cu(H2O)6]2+.
CH tr 117 TL2
Trả lời câu hỏi Thảo luận 2 trang 117 SGK Hóa 12 Chân trời sáng tạo
Viết phương trình hoá học của phản ứng xảy ra khi hoà tan kết tủa Cu(OH)2 bằng dung dịch ammonia.
Phương pháp giải:
Khi cho đến dư dung dịch ammonia vào kết tủa Cu(OH)2, kết tủa tan, tạo thành dung dịch màu xanh lam chứa ion phức [Cu(NH3)4(H2O)2]2+, thường viết là [Cu(NH3)4]2+.
Lời giải chi tiết:
\({\rm{Cu}}{\left( {{\rm{OH}}} \right)_{\rm{2}}} + {\rm{ }}4{\rm{N}}{{\rm{H}}_{\rm{3}}} \to \left[ {{\rm{Cu}}{{\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)}_{\rm{4}}}} \right]{({\rm{OH)}}_{\rm{2}}}\)
CH tr 117 TL3
Trả lời câu hỏi Thảo luận 3 trang 117 SGK Hóa 12 Chân trời sáng tạo
Nêu các hiện tượng quan sát được ở Thí nghiệm 1. Viết phương trình hoá học của phản ứng xảy ra trong thí nghiệm và giải thích.
Phương pháp giải:
Chẳng hạn khi hoà tan CuSO4 vào nước tạo thành phức chất aqua [Cu(H2O)6]2+. Có màu xanh. Khi nhỏ thêm vài giọt dung dịch kiềm sẽ tạo thành kết tủa xanh nhạt Cu(OH)2. Khi cho đến dư dung dịch ammonia vào kết tủa Cu(OH)2, kết tủa tan, tạo thành dung dịch màu xanh lam chứa ion phức [Cu(NH3)4(H2O)2]2+, thường viết là [Cu(NH3)4]2+.
Lời giải chi tiết:
- Hiện tượng: Ban đầu xuất hiện kết tủa xanh, sau đó kết tủa xanh tan thành dung dịch xanh lam.
- Giải thích:
+ Ban đầu, khi nhỏ dung dịch NH3 vào dung dịch CuSO4 thì xuất hiện kết tủa xanh Cu(OH)2.
\({{\mathop{\rm CuSO}\nolimits} _4} + 2{\rm{N}}{{\rm{H}}_{\rm{3}}} + 2{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{Cu(OH}}{{\rm{)}}_{\rm{2}}} \downarrow + {\rm{ (N}}{{\rm{H}}_{\rm{4}}}{{\rm{)}}_{\rm{2}}}{\rm{S}}{{\rm{O}}_{\rm{4}}}\)
+ Tiếp tục nhỏ dung dịch NH3 đến dư, kết tủa xanh Cu(OH)2 tan trong dung dịch NH3 tạp phức chất màu xanh lam \(\left[ {{\rm{Cu}}{{\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)}_{\rm{4}}}} \right]{({\rm{OH)}}_{\rm{2}}}\).
\({\rm{Cu}}{\left( {{\rm{OH}}} \right)_{\rm{2}}} + {\rm{ }}4{\rm{N}}{{\rm{H}}_{\rm{3}}} \to \left[ {{\rm{Cu}}{{\left( {{\rm{N}}{{\rm{H}}_{\rm{3}}}} \right)}_{\rm{4}}}} \right]{({\rm{OH)}}_{\rm{2}}}\)
CH tr 118 TL1
Trả lời câu hỏi Thảo luận 1 trang 118 SGK Hóa 12 Chân trời sáng tạo
Nêu các hiện tượng quan sát được ở Thí nghiệm 2. Viết phương trình hoá học của phản ứng xảy ra trong thí nghiệm.
Phương pháp giải:
Trong dung dịch CuSO4 ở dạng phức chất aqua [Cu(H2O)6]2+ màu xanh, khi nhỏ thêm dung dịch HCl thì xảy ra phản ứng thế phối tử của phức chất trong dung dịch.
Lời giải chi tiết:
- Hiện tượng: Dung dịch màu xanh đổi màu thành dung dịch màu vàng.
- Phương trình hóa học: \({\left[ {{\rm{Cu}}{{\left( {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right)}_{\rm{6}}}} \right]^{{\rm{2 + }}}} + {\rm{4C}}{{\rm{l}}^ - } \to {\left[ {{\rm{CuC}}{{\rm{l}}_{\rm{4}}}} \right]^{{\rm{2 - }}}} + 6{{\rm{H}}_{\rm{2}}}{\rm{O}}\)
CH tr 118 TL2
Trả lời câu hỏi Thảo luận 2 trang 118 SGK Hóa 12 Chân trời sáng tạo
Em hãy vẽ sơ đó tư duy mô tả một số ứng dụng của phức chất.
Phương pháp giải:
Em hãy vẽ sơ đó tư duy mô tả một số ứng dụng của phức chất.
Lời giải chi tiết:
Em hãy vẽ sơ đó tư duy mô tả một số ứng dụng của phức chất.
CH tr 119 VD
Trả lời câu hỏi Vận dụng trang 119 SGK Hóa 12 Chân trời sáng tạo
Bằng kiến thức đã học, em hãy thiết kế poster trình bày một số ứng dụng của phức chất trong y học, dược học và hoá học.
Phương pháp giải:
Dựa vào các thông tin được nêu trong mục 4 trang 118 sách giáo khoa.
Lời giải chi tiết:
Học sinh tự vẽ poster với các từ khóa được tìm kiếm trong mục 4 trang 118 sách giáo khoa.
CH tr 119 BT1
Trả lời câu hỏi Bài tập 1 trang 119 SGK Hóa 12 Chân trời sáng tạo
Trong phức chất, giữa phối tử và nguyên tử trung tâm có loại liên kết nào sau đây?
A. Ion. B. Hydrogen. C. cho - nhận. D. Kim loại.
Phương pháp giải:
Liên kết giữa phối tử và nguyên tử trung tâm là liên kết cho – nhận.
Lời giải chi tiết:
Trong phức chất, giữa phối tử và nguyên tử trung tâm có loại liên kết cho – nhận.
→ Chọn C.
CH tr 119 BT2
Trả lời câu hỏi Bài tập 2 trang 119 SGK Hóa 12 Chân trời sáng tạo
Viết công thức hoá học các phức chất aqua của ion Mn2+ và ion Co3+. Biết chúng đều có dạng hình học bát diện.
Phương pháp giải:
Hầu hết phức chất aqua của ion kim loại chuyển tiếp dãy thứ nhất đều có màu. chúng thường có dạng [M(H2O)6]n+.
Lời giải chi tiết:
Công thức phức chất aqua của ion Mn2+ là [Mn(H2O)6]2+.
Công thức phức chất aqua của ion Co3+ là [Co(H2O)6]3+.
CH tr 119 BT3
Trả lời câu hỏi Bài tập 3 trang 119 SGK Hóa 12 Chân trời sáng tạo
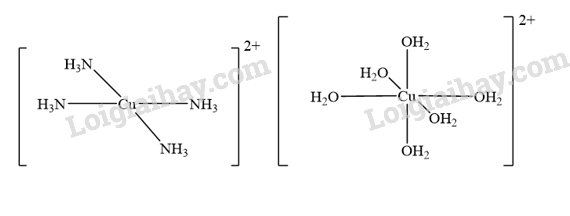
lon [Cu(NH3)4]2+ có dạng vuông phẳng, ion [Cu(H2O)6]2+ có dạng bát diện. Hãy vẽ dạng hình học của chúng.
Phương pháp giải:
Lời giải chi tiết:
Các bài khác cùng chuyên mục
- Bài 20. Sơ lược về phức chất và sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch trang 115, 116, 117 Hóa 12 Chân trời sáng tạo
- Bài 19. Đại cương về kim loại chuyển tiếp dãy thứ nhất trang 110, 111, 112 Hóa 12 Chân trời sáng tạo
- Bài 18. Nguyên tố nhóm IIA trang 100, 101, 102 Hóa 12 Kết nối tri thức
- Bài 17. Nguyên tố nhóm IA trang 91, 92, 93 Hóa 12 Chân trời sáng tạo
- Bài 16. Hợp kim và sự ăn mòn kim loại trang 85, 86, 87 Hóa 12 Chân trời sáng tạo
- Bài 20. Sơ lược về phức chất và sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch trang 115, 116, 117 Hóa 12 Chân trời sáng tạo
- Bài 19. Đại cương về kim loại chuyển tiếp dãy thứ nhất trang 110, 111, 112 Hóa 12 Chân trời sáng tạo
- Bài 18. Nguyên tố nhóm IIA trang 100, 101, 102 Hóa 12 Kết nối tri thức
- Bài 17. Nguyên tố nhóm IA trang 91, 92, 93 Hóa 12 Chân trời sáng tạo
- Bài 16. Hợp kim và sự ăn mòn kim loại trang 85, 86, 87 Hóa 12 Chân trời sáng tạo









