Lý thuyết cấu tạo phân tử hợp chất hữu cơ
I. ĐẶC ĐIỂM CẤU TẠO PHÂN TỬ HỢP CHẤT HỮU CƠ
I. ĐẶC ĐIỂM CẤU TẠO PHÂN TỬ HỢP CHẤT HỮU CƠ
1. Hóa trị và liên kết giữa các nguyên tử
- Trong các hợp chất hữu cơ, cacbon luôn có hóa trị IV, hiđro có hóa trị I, oxi có hóa trị II. (mỗi hóa trị được biểu diễn bằng một gạch nối giữa hai nguyên tử liên kết)
- Các nguyên tử liên kết với nhau theo đúng hóa trị của chúng. Mỗi liên kết được biểu diễn bằng một nét gạch nối giữa hai nguyên tử.
- Ví dụ với phân tử CH4 :
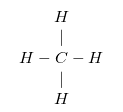
2. Mạch cacbon
- Những nguyên tử cacbon trong phân tử hợp chất hữu cơ có thể liên kết trực tiếp với nhau tạo thành mạch cacbon.
- Có 3 loại mạch cacbon:
+ Mạch không phân nhánh (mạch thẳng).
+ Mạch nhánh.
+ Mạch vòng.
3. Trật tự liên kết giữa các nguyên tử trong phân tử
- Mỗi hợp chất hữu cơ có một trật tự liên kết giữa các nguyên tử trong phân tử.
- Ví dụ cùng công thức phân tử C2H6O có 2 chất:

rượu etylic (chất lỏng)
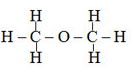
đimetyl ete (chất khí)
II. CÔNG THỨC CẤU TẠO
- Công thức biểu diễn đầy đủ liên kết giữa các nguyên tử trong phân tử gọi là công thức cấu tạo
- Ví dụ: Công thức cấu tạo của etan:
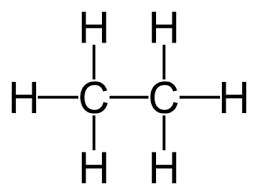 viết gọn CH3 – CH3
viết gọn CH3 – CH3
- Công thức cấu tạo cho biết thành phần của phân tử và trật tự liên kết giữa các nguyên tử trong phân tử.
Sơ đồ tư duy: Cấu tạo phân tử hợp chất hữu cơ
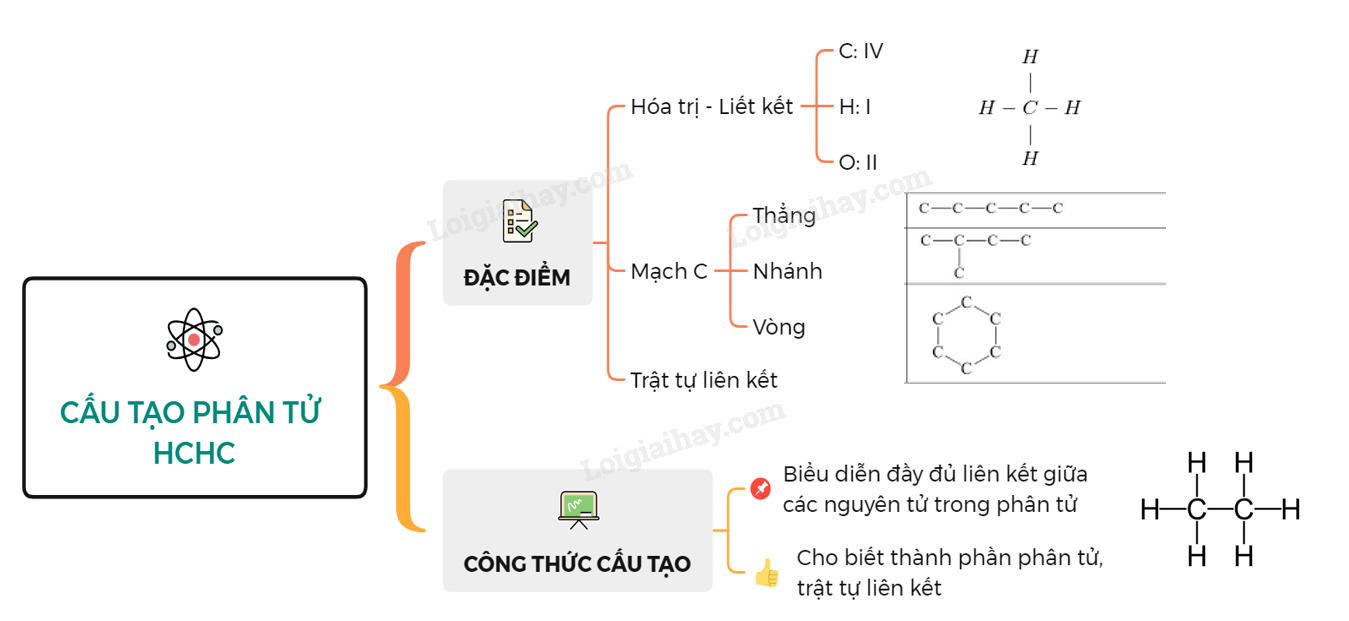
Loigiaihay.com
- Bài 1 trang 112 SGK Hoá học 9
- Bài 2 trang 112 SGK Hoá học 9
- Bài 3 trang 112 SGK Hoá học 9
- Bài 4 trang 112 SGK Hoá học 9
- Bài 5 trang 112 SGK Hoá học 9
>> Xem thêm
Các bài khác cùng chuyên mục
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu


















